题目内容
(共7分)欲配制 250 mL0.1 mol·L-1的NaOH溶液,回答下列问题:
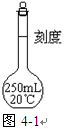
(1)写出图4-1仪器的名称 ,使用此仪器前要检查它是否 。
(2)用托盘天平称取NaOH固体的质量 g。
(3)转移溶液时,应将已冷却的NaOH溶液沿 注入右图所示的仪器中。
(4)若称量前NaOH已部分潮解,则配制的溶液的浓度 (偏大或偏小)。
(5)在配制该NaOH溶液时必须用到的实验仪器是(填序号) 。(2分)
①500mL的量筒 ②烧杯 ③托盘天平 ④250mL的容量瓶 ⑤玻璃棒
⑥1000mL的容量瓶 ⑦胶头滴管 ⑧250mL的量筒

(1)写出图4-1仪器的名称 ,使用此仪器前要检查它是否 。
(2)用托盘天平称取NaOH固体的质量 g。
(3)转移溶液时,应将已冷却的NaOH溶液沿 注入右图所示的仪器中。
(4)若称量前NaOH已部分潮解,则配制的溶液的浓度 (偏大或偏小)。
(5)在配制该NaOH溶液时必须用到的实验仪器是(填序号) 。(2分)
①500mL的量筒 ②烧杯 ③托盘天平 ④250mL的容量瓶 ⑤玻璃棒
⑥1000mL的容量瓶 ⑦胶头滴管 ⑧250mL的量筒
(1)容量瓶,漏水;(3)玻璃棒;(4)偏小
(2)1.0; (5)②③④⑤⑦
(2)1.0; (5)②③④⑤⑦
略

练习册系列答案
相关题目
 -
-


 Cu2+、NH4+、K+、CO32-、SO42-等离子的几种,为分析其成分,取此溶液分别进行了四个实验,其操作和有关现象如
Cu2+、NH4+、K+、CO32-、SO42-等离子的几种,为分析其成分,取此溶液分别进行了四个实验,其操作和有关现象如 下图所示:
下图所示: