题目内容
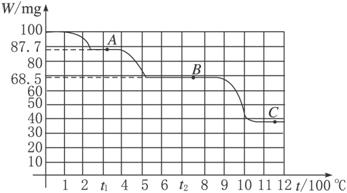
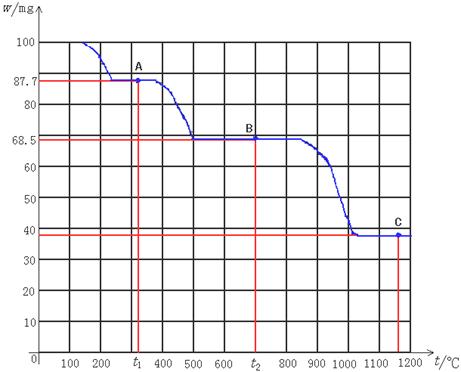
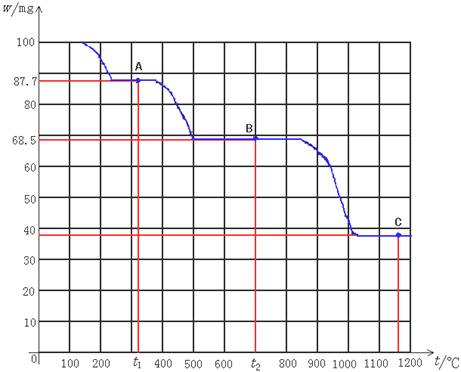
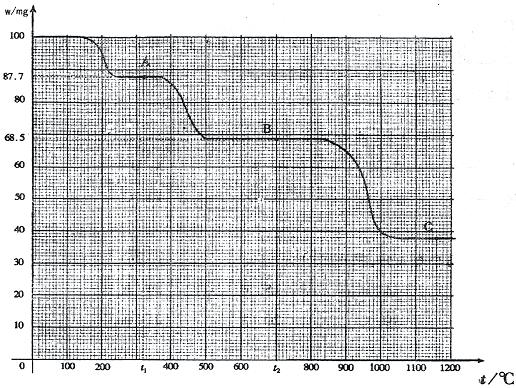
下图是100 mg CaC2O4·H2O受热分解时,所得固体产物的质量随温度变化的曲线。试利用图中信息结合所学的知识,回答下列各问题: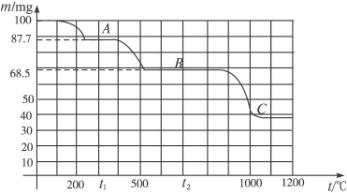
(1)温度分别为t1和t2时,固体产物的化学式A是______________,B是______________。
(2)由CaC2O4·H2O得到A的化学方程式为__________________________________。
(3)由A得到B的化学方程式为____________________________________________。
(4)由图计算产物C的相对分子质量,并推断C的合理的化学式。
(1)CaC2O4 CaCO3
(2)CaC2O4·H2O![]() CaC2O4+H2O↑
CaC2O4+H2O↑
(3)CaC2O4![]() CaCO3+CO↑
CaCO3+CO↑
(4)56 CaO
解析:CaC2O4·H2O在加热时可能发生以下反应:
CaC2O4·H2O![]() CaC2O4+H2O↑ CaC2O4
CaC2O4+H2O↑ CaC2O4![]() CaCO3+CO↑ CaCO3
CaCO3+CO↑ CaCO3![]() CaO+CO2↑。
CaO+CO2↑。
根据钙原子守恒得如下关系式,并计算各固体残留物的预期质量:
CaC2O4·H2O — CaC2O4 — CaCO3 — CaO
146000 mg 128000 mg 100000 mg 56000 mg
100 mg ?=87.7 mg ?=68.5 mg ?=38.3 mg
计算出来的各固体残留物的预期质量与图象所示的实验数据相符,说明受热时确实是按照上述方程式进行反应的,所以A是CaC2O4,B是CaCO3,C是CaO。

练习册系列答案
相关题目