题目内容
 (1)一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ?mol-1)的变化.关于该反应的下列说法中,正确的是
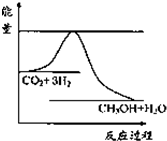
(1)一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ?mol-1)的变化.关于该反应的下列说法中,正确的是A.△H>0,△S>0 B.△H>0,△S<0
C.△H<0,△S<0 D.△H<0,△S>0
(2)由氢气和氧气反应生成1mol水蒸气时,放出热量241.8kJ,写出该反应的热化学方程式
(3)写出乙醇在催化剂下催化氧化生成乙醛的化学方程式
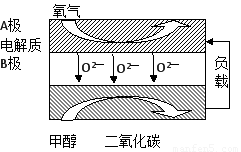
(4)将两个石墨电极插人KOH溶液中,向两极分别通入H2和O2,构成氢气燃料电池.通入O2的一极,其电极反应式是:O2+4e-+2H2O=4OH-;通入H2的一极,其电极反应式是
分析:(1)依据图象分析可知反应中反应物能量高于生成物反应是放热反应,反应前后气体体积减小熵变小于0;
(2)依据热化学方程式书写方法,标注物质聚集状态和对饮反应的焓变写出;
(3)乙醇催化氧化生成乙醛和水,配平书写化学方程式;
(4)氢氧燃料电池中通氢气的一极在原电池负极失电子发生氧化反应.
(2)依据热化学方程式书写方法,标注物质聚集状态和对饮反应的焓变写出;
(3)乙醇催化氧化生成乙醛和水,配平书写化学方程式;
(4)氢氧燃料电池中通氢气的一极在原电池负极失电子发生氧化反应.
解答:解:(1)依据图象分析可知反应中反应物能量高于生成物反应是放热反应,△H<0,反应前后气体体积减小熵变小于0,△S<0;
故答案为:C;
(2)依据热化学方程式书写方法,标注物质聚集状态和对饮反应的焓变写出,氢气和氧气反应生成1mol水蒸气时,放出热量241.8kJ,热化学方程式
H2(g)+
O2(g)=H2O(g),△H=-241.8KJ/mol;
故答案为:H2(g)+
O2(g)=H2O(g),△H=-241.8KJ/mol;
(3)乙醇催化氧化生成乙醛和水,反应化学方程式,2CH3CH2OH+O2
2CH3CHO+2H2O;
故答案为:2CH3CH2OH+O2
2CH3CHO+2H2O;
(4)氢氧燃料电池中通氢气的一极在原电池负极失电子发生氧化反应,碱溶液中生成水,电极反应为H2-2e-+2OH-=2H2O,故答案为:H2-2e-+2OH-=2H2O.
故答案为:C;
(2)依据热化学方程式书写方法,标注物质聚集状态和对饮反应的焓变写出,氢气和氧气反应生成1mol水蒸气时,放出热量241.8kJ,热化学方程式
H2(g)+
| 1 |
| 2 |
故答案为:H2(g)+
| 1 |
| 2 |
(3)乙醇催化氧化生成乙醛和水,反应化学方程式,2CH3CH2OH+O2
| 催化剂 |
| △ |
故答案为:2CH3CH2OH+O2
| 催化剂 |
| △ |
(4)氢氧燃料电池中通氢气的一极在原电池负极失电子发生氧化反应,碱溶液中生成水,电极反应为H2-2e-+2OH-=2H2O,故答案为:H2-2e-+2OH-=2H2O.
点评:本题考查了图象分析,热化学方程式书写方法,原电池原理的分析应用,电极反应书写方法,掌握基础是关键.

练习册系列答案
相关题目