题目内容
下列溶液中有关离子浓度的说法可能正确的是( )A.NH4Cl溶液:c(Cl-)>c(NH
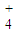 )>c(OH-)>c(H+)
)>c(OH-)>c(H+)B.Na2CO3溶液中:c(Na+)+c(H+)=c(HCO
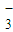 )+c(OH-)+c(CO
)+c(OH-)+c(CO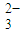 )
)C.等物质的量的CH3COOH与NaOH混合溶液中:c(CH3COO-)=c(Na+)=c(H+)=c(OH-)
D.在NaHCO3溶液中:c(Na+)=c(HCO
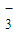 )+c(CO
)+c(CO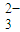 )+c(H2CO3)
)+c(H2CO3)
【答案】分析:A、氯化铵溶液中铵根离子水解显酸性;
B、依据溶液中电荷守恒计算分析判断;
C、等物质的量CH3COOH与NaOH混合反应生成醋酸钠和水,醋酸根离子水解溶液显碱性;
D、依据溶液中的物料守恒分析判断;
解答:解:A、氯化铵溶液中铵根离子水解显酸性,溶液中离子浓度大小为:c(Cl-)>c(NH4+)>c(H+)>c(OH-);故A错误;
B、Na2CO3溶液中存在电荷守恒:c(Na+)+c(H+)=c(HCO3-)+c(OH-)+2c(CO32-);故B错误;
C、等物质的量的CH3COOH与NaOH混合反应生成醋酸钠和水,醋酸根离子水解溶液显碱性,溶液中c(Na+)>c(CH3COO-)>c(OH-)>c(H+);故C错误;
D、在NaHCO3溶液中n(Na)=n(C),溶液中电荷守恒得到:c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3);故D正确;
故选D.
点评:本题考查离子浓度的大小比较,题目难度中等,注意把握弱电解质的电离和盐类水解的原理,从守恒的角度比较离子浓度大小是常用的方法.
B、依据溶液中电荷守恒计算分析判断;
C、等物质的量CH3COOH与NaOH混合反应生成醋酸钠和水,醋酸根离子水解溶液显碱性;
D、依据溶液中的物料守恒分析判断;
解答:解:A、氯化铵溶液中铵根离子水解显酸性,溶液中离子浓度大小为:c(Cl-)>c(NH4+)>c(H+)>c(OH-);故A错误;
B、Na2CO3溶液中存在电荷守恒:c(Na+)+c(H+)=c(HCO3-)+c(OH-)+2c(CO32-);故B错误;
C、等物质的量的CH3COOH与NaOH混合反应生成醋酸钠和水,醋酸根离子水解溶液显碱性,溶液中c(Na+)>c(CH3COO-)>c(OH-)>c(H+);故C错误;
D、在NaHCO3溶液中n(Na)=n(C),溶液中电荷守恒得到:c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3);故D正确;
故选D.
点评:本题考查离子浓度的大小比较,题目难度中等,注意把握弱电解质的电离和盐类水解的原理,从守恒的角度比较离子浓度大小是常用的方法.

练习册系列答案
 53天天练系列答案
53天天练系列答案
相关题目
 (用离子方程式表示),
(用离子方程式表示),