题目内容
CuSO4是一种重要的化工原料
(1)在粗制CuSO4?5H2O晶体中常含有杂质Fe2+.在提纯时为了除去Fe2+,常加入合适氧化剂,使Fe2+氧化为Fe3+,下列物质可采用的是
A.KMnO4 B.双氧水 C.氯水 D.HNO3
然后再加入适当物质调整至溶液pH=4,使Fe3+转化为Fe(OH)3,可以达到除去Fe3+而不损失CuSO4的目的,调整溶液pH可选用下列中的
A.NaOH B.氨水 C.CuO D.Cu(OH)2
(2)甲同学怀疑调整至溶液pH=4是否能达到除去Fe3+而不损失Cu2+的目的,乙同学认为可以通过计算确定,他查阅有关资料得到如下数据,常温下Fe(OH)3的溶度积Ksp=8.0×10-38,Cu(OH)2的溶度积Ksp=3.0×10-20,通常认为残留在溶液中的离子浓度小于1×10-5 mol?L-1时就认为沉淀完全,设溶液中CuSO4的浓度为3.0mol?L-1,则Cu(OH)2开始沉淀时溶液的pH为
(3)硫酸铜晶体的溶解度虽大,但溶解过程较慢,实验室常用热水配制以加快溶解速率,但常常会产生浑浊,请用文字简要说明原因
(1)在粗制CuSO4?5H2O晶体中常含有杂质Fe2+.在提纯时为了除去Fe2+,常加入合适氧化剂,使Fe2+氧化为Fe3+,下列物质可采用的是
B
B
.(用符号表示,下同)A.KMnO4 B.双氧水 C.氯水 D.HNO3
然后再加入适当物质调整至溶液pH=4,使Fe3+转化为Fe(OH)3,可以达到除去Fe3+而不损失CuSO4的目的,调整溶液pH可选用下列中的
CD
CD
.A.NaOH B.氨水 C.CuO D.Cu(OH)2
(2)甲同学怀疑调整至溶液pH=4是否能达到除去Fe3+而不损失Cu2+的目的,乙同学认为可以通过计算确定,他查阅有关资料得到如下数据,常温下Fe(OH)3的溶度积Ksp=8.0×10-38,Cu(OH)2的溶度积Ksp=3.0×10-20,通常认为残留在溶液中的离子浓度小于1×10-5 mol?L-1时就认为沉淀完全,设溶液中CuSO4的浓度为3.0mol?L-1,则Cu(OH)2开始沉淀时溶液的pH为
4
4
,Fe3+完全沉淀时溶液的pH为3.3
3.3
,通过计算确定上述方案可行
可行
(填“可行”或“不可行”).(3)硫酸铜晶体的溶解度虽大,但溶解过程较慢,实验室常用热水配制以加快溶解速率,但常常会产生浑浊,请用文字简要说明原因
Cu2+水解产生Cu(OH)2是吸热反应,加热促进水解,故产生浑浊
Cu2+水解产生Cu(OH)2是吸热反应,加热促进水解,故产生浑浊
,如何才能用热水配制出澄清的较浓的CuSO4溶液应加入少量H2SO4
应加入少量H2SO4
.分析:(1)根据除杂质至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质,调整溶液的pH时,加入的物质不能引进新的杂质粒子.以此来解答;
(2)依据氢氧化铜饱和溶液中溶度积常数计算溶液中的氢离子浓度计算PH;结合氢氧化铁溶度积和残留在溶液中的离子浓度小于1×10-5 mol?L-1时就认为沉淀完全;
(3)根据盐类的水解是吸热过程以及升温对平衡的影响来解答;根据生成物浓度对水解平衡的影响来解答.
(2)依据氢氧化铜饱和溶液中溶度积常数计算溶液中的氢离子浓度计算PH;结合氢氧化铁溶度积和残留在溶液中的离子浓度小于1×10-5 mol?L-1时就认为沉淀完全;
(3)根据盐类的水解是吸热过程以及升温对平衡的影响来解答;根据生成物浓度对水解平衡的影响来解答.
解答:解:(1)除杂质至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质,四个选项中,只有双氧水氧化后生成水,双氧水受热见光易分解,没有多余杂质;调整溶液的pH时,加入的物质不能引进新的杂质粒子,氢氧化钠中含有钠离子,氨水反应后生成铵根离子,所以氢氧化钠和氨水能引进新的杂质离子,CuO粉末、Cu(OH)2悬浊液反应后生成铜离子和水而不引进新的杂质离子,故选CD.
故答案为:B;CD;
(2)Cu(OH)2的溶度积Ksp=3.0×10-20,溶液中CuSO4的浓度为3.0mol?L-1,c(Cu2+)=3.0mol?L-1;依据溶度积常数c(Cu2+)×c2(OH-)=3.0×10-20 ;c2(OH-)=
=10-22;得到c(OH-)=10-10mol/L,依据水溶液中的离子积c(H+)×c(OH-)=10-14;求的c(H+)=10-4mol/L,溶液pH=4,则Cu(OH)2开始沉淀时溶液的pH为4;残留在溶液中的离子浓度小于1×10-5 mol?L-1时就认为沉淀完全,Fe(OH)3的溶度积Ksp=8.0×10-38,c(Fe3+)×c3(OH-)=8.0×10-38;c3(OH-)=
=8.0×10-33;求的c(OH-)=2×10-11mol/L;水溶液中的离子积c(H+)×c(OH-)=10-14;c(H+)=5×10-4mol/L,则pH=3.3;通过计算可知pH=4能达到除去Fe3+而不损失Cu2+的目的,则方案可行,
故答案为:4;3.3;可行.
(3)因Cu2+水解产生Cu(OH)2,该反应是吸热反应,加热促进水解,故产生浑浊;硫酸浓度增大,平衡逆向移动,能得到澄清的较浓的CuSO4溶液,
故答案为:Cu2+水解产生Cu(OH)2是吸热反应,加热促进水解,故产生浑浊;应加入少量H2SO4.
故答案为:B;CD;
(2)Cu(OH)2的溶度积Ksp=3.0×10-20,溶液中CuSO4的浓度为3.0mol?L-1,c(Cu2+)=3.0mol?L-1;依据溶度积常数c(Cu2+)×c2(OH-)=3.0×10-20 ;c2(OH-)=
| 3×10-20 |
| 3.0 |
| 8.0×10-38 |
| 1×10-5 |
故答案为:4;3.3;可行.
(3)因Cu2+水解产生Cu(OH)2,该反应是吸热反应,加热促进水解,故产生浑浊;硫酸浓度增大,平衡逆向移动,能得到澄清的较浓的CuSO4溶液,
故答案为:Cu2+水解产生Cu(OH)2是吸热反应,加热促进水解,故产生浑浊;应加入少量H2SO4.
点评:本题考查了沉淀转化的原理应用,除杂的原理应用,主要是溶解沉淀的转化关系的分析应用和计算,题目难度中等.

练习册系列答案
相关题目
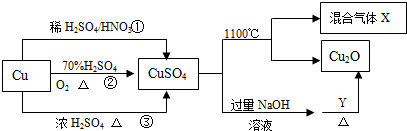
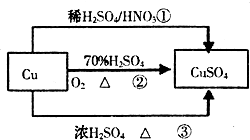 CuSO4是一种重要的化工原料,有关制备途径及性质如图所示.下列说法错误的是( )
CuSO4是一种重要的化工原料,有关制备途径及性质如图所示.下列说法错误的是( )| A、途径①所用混酸中H2SO4与HNO3物质的量之比最好为3:2 | B、相对于途径①、③,途径②更好地体现了绿色化学思想 | C、生成等量的硫酸铜,三个途径中参加反应的硫酸的物质的量:①=②<③ | D、利用途径②制备16g硫酸铜,被还原的硫酸的物质的量为0.1mol |
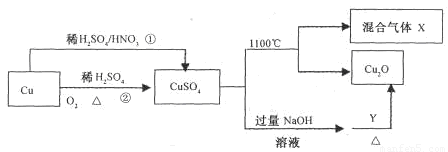
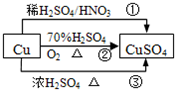 CuSO4是一种重要的化工原料,其有关制备途径如图所示.下列说法不正确的是( )
CuSO4是一种重要的化工原料,其有关制备途径如图所示.下列说法不正确的是( )(已知:2Cu+O2+2H2SO4→2CuSO4+2H2O)
| A、相对于途径①、③,途径②更好地体现了绿色化学思想 | B、途径③中,1mol Cu与足量浓硫酸反应会产生64g SO2气体 | C、途径①所用混酸中H2SO4与HNO3物质的量之比最好为3:2 | D、1mol Cu分别按照途径②、③中,被还原的H2SO4的质量之比为1:1 |