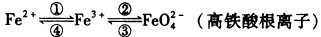题目内容
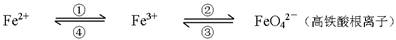
铁及其化合物之间的相互转化可用下式表示:Fe2+
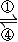 Fe3+
Fe3+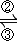 FeO42-(高铁酸根离子)
FeO42-(高铁酸根离子)回答下列有关问题:
(1)Fe与过量稀硫酸反应可以制取FeSO4.若用反应所得的酸性溶液,实现上述①的转化,要求产物纯净.可选用的试剂是______(选填序号);
a.Cl2 b.Fe c.HNO3 d.H2O2
(2)上述转化得到的硫酸铁可用于电化浸出黄铜矿精矿工艺.精矿在阳极浸出的反应比较复杂,其中有一主要反应:CuFeS2+4Fe3+=Cu2++5Fe2++2S.(CuFeS2中S为-2价)则下列说法正确的是______(选填序号);
a.从物质分类的角度看,黄铜矿属于合金
b.反应中,所有铁元素均被还原
c.反应中,CuFeS2 既作氧化剂又作还原剂
d.当转移1mol电子时,46g CuFeS2参加反应
(3)下述反应中,若FeSO4和O2的系数比为2:1,试配平下列方程式:FeSO4+K2O2→K2FeO4+K2O+K2SO4+O2↑
(4)高铁酸钾(K2FeO4)是一种新型、高效的绿色水处理剂,在水中发生反应生成Fe(OH)3.高铁酸钾作为水处理剂发挥的作用是______、______.
【答案】分析:(1)根据物质的性质及是否引进杂质确定选项;
(2)根据合金的定义、化合价的升降、发生反应的物质与转移电子之间的关系判断;
(3)根据得失电子数相等配平反应方程式,注意化合价的判断方法;
(4)利用离子的水解产物的性质来分析净水原因.
解答:解:(1)要使产物纯净,必须物质间发生反应后,没有杂质生成.
a、氯气有氧化性,能氧化二价铁离子生成三价铁离子,但同时有氯离子生成,所以有杂质生成,故a错误;
b、铁与稀硫酸反应生成二价铁离子,不能把二价铁离子转化为三价铁离子,故b错误;
c、硝酸能氧化二价铁离子生成三价铁离子,但溶液中还有杂质硝酸根离子,故c错误;
d、双氧水能氧化二价铁离子生成三价铁离子,同时有水生成,水是原溶液的成分,所以不是杂质,故d正确;
故选d;
(2)a、合金是由两种或两种以上的金属与非金属经一定方法所合成的具有金属特性的物质,所以黄铜矿不是合金,故a错误;
b、CuFeS2中铁元素的化合价为+2价,反应物Fe3+的化合价为+3价,生成物中Fe2+的化合价为+2价,所以不是所有铁元素均被还原,故b错误;
c、CuFeS2中只有S元素的化合价只有升高,其他元素的化合价不变,所以CuFeS2只作还原剂,故c错误;
d、CuFeS2+4Fe3+=Cu2++5Fe2++2S 转移电子4
184g 4mol
46g 1mol
故d正确;
故选d;
(3)FeSO4+K2O2→K2FeO4+K2O+K2SO4+O2↑,该反应,FeSO4中Fe的化合价为+2价,K2FeO4中Fe的化合价为+6价,所以一个氯化亚铁分子失去4个电子;K2O2中O的化合价为-1价,O2中O的化合价为0价,一个K2O2分子失去2个电子生成氧气;K2O2中O的化合价为-1价,K2FeO4和K2O中O元素的化合价为-2价,所以一个K2O2失去2个电子,该方程式中得失电子的最小公倍数为6,所以该方程式的计量数分别为2、6、2、2、2、1,即方程式为2FeSO4+6K2O2=2K2FeO4+2K2O+2K2SO4+1O2↑,
故答案为:2、6、2、2、2、1;
(4)高铁酸钾( K2FeO4)中Fe的化合价是+6价,具有强氧化性,能杀菌消毒,其还原产物Fe3+水解生成氢氧化铁胶体,能吸附水中杂质,所以高铁酸钾作为水处理剂发挥的作用是净水、消毒,故答案为:净水;消毒.
点评:本题考查了铁盐和亚铁盐的相互转化,难度不大,注意二价铁离子和三价铁离子的检验是高考的热点,三价铁离子能使KSCN变红色.
(2)根据合金的定义、化合价的升降、发生反应的物质与转移电子之间的关系判断;
(3)根据得失电子数相等配平反应方程式,注意化合价的判断方法;
(4)利用离子的水解产物的性质来分析净水原因.
解答:解:(1)要使产物纯净,必须物质间发生反应后,没有杂质生成.
a、氯气有氧化性,能氧化二价铁离子生成三价铁离子,但同时有氯离子生成,所以有杂质生成,故a错误;
b、铁与稀硫酸反应生成二价铁离子,不能把二价铁离子转化为三价铁离子,故b错误;
c、硝酸能氧化二价铁离子生成三价铁离子,但溶液中还有杂质硝酸根离子,故c错误;
d、双氧水能氧化二价铁离子生成三价铁离子,同时有水生成,水是原溶液的成分,所以不是杂质,故d正确;
故选d;
(2)a、合金是由两种或两种以上的金属与非金属经一定方法所合成的具有金属特性的物质,所以黄铜矿不是合金,故a错误;
b、CuFeS2中铁元素的化合价为+2价,反应物Fe3+的化合价为+3价,生成物中Fe2+的化合价为+2价,所以不是所有铁元素均被还原,故b错误;
c、CuFeS2中只有S元素的化合价只有升高,其他元素的化合价不变,所以CuFeS2只作还原剂,故c错误;
d、CuFeS2+4Fe3+=Cu2++5Fe2++2S 转移电子4
184g 4mol
46g 1mol
故d正确;
故选d;
(3)FeSO4+K2O2→K2FeO4+K2O+K2SO4+O2↑,该反应,FeSO4中Fe的化合价为+2价,K2FeO4中Fe的化合价为+6价,所以一个氯化亚铁分子失去4个电子;K2O2中O的化合价为-1价,O2中O的化合价为0价,一个K2O2分子失去2个电子生成氧气;K2O2中O的化合价为-1价,K2FeO4和K2O中O元素的化合价为-2价,所以一个K2O2失去2个电子,该方程式中得失电子的最小公倍数为6,所以该方程式的计量数分别为2、6、2、2、2、1,即方程式为2FeSO4+6K2O2=2K2FeO4+2K2O+2K2SO4+1O2↑,
故答案为:2、6、2、2、2、1;
(4)高铁酸钾( K2FeO4)中Fe的化合价是+6价,具有强氧化性,能杀菌消毒,其还原产物Fe3+水解生成氢氧化铁胶体,能吸附水中杂质,所以高铁酸钾作为水处理剂发挥的作用是净水、消毒,故答案为:净水;消毒.
点评:本题考查了铁盐和亚铁盐的相互转化,难度不大,注意二价铁离子和三价铁离子的检验是高考的热点,三价铁离子能使KSCN变红色.

练习册系列答案
相关题目
 铁及其化合物之间的相互转化可用下式表示:①②③④
铁及其化合物之间的相互转化可用下式表示:①②③④