题目内容
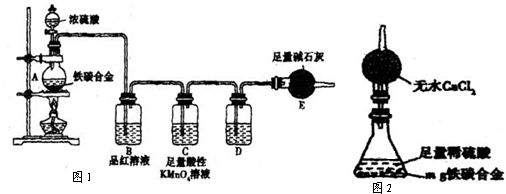
某化学实验小组为了除去混在N2中的O2,将混合气体通过红热的铜丝网后,发现铜丝网变黑.在研究如何除去黑色物质,回收再利用铜丝网的讨论中,实验小组制定了下列两套实验方案:

请根据以上方案回答:
(1)乙方案的烧杯中发生反应的化学方程式是(其中B物质自行确定)________.
两种方案相比较,甲方案明显的不足之处有(a):________(b):________.
(2)若采用甲乙两种方案处理此黑色铜丝网,则回收的铜丝网a的质量________(填“<”、“>”、“=”)铜丝网b的质量.原因是:________
(3)实验小组同学发现,按乙方案反应后烧杯中的液体有腐蚀性,应加以适当的处理.他们采取加入铁粉的方案处理废液.加入足量的铁粉充分搅拌,最后得到的溶液中溶质为________(写化学式).
答案:
解析:
解析:
|
(1)CuO+H2SO4 (2)>,略 (3)FeSO4(其他合理答案也可). |

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目



 饱和氯水与石灰石的反应是制取较浓HClO溶液的方法之一.某化学实验小组先制取氯气,后将其溶于水制成饱和氯水,并进行了如下定性研究:
饱和氯水与石灰石的反应是制取较浓HClO溶液的方法之一.某化学实验小组先制取氯气,后将其溶于水制成饱和氯水,并进行了如下定性研究: