题目内容
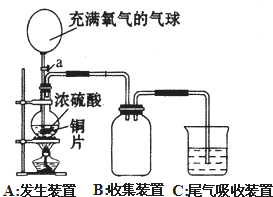 小明同学设计了如图所示装置来探究铜跟浓硫酸的反应.先关闭活塞a,加热至烧杯中不再有气泡产生时,停止反应,此时烧瓶中铜片仍有剩余.再打开活塞a,将气球中的氧气缓缓挤入烧瓶,铜片慢慢消失.
小明同学设计了如图所示装置来探究铜跟浓硫酸的反应.先关闭活塞a,加热至烧杯中不再有气泡产生时,停止反应,此时烧瓶中铜片仍有剩余.再打开活塞a,将气球中的氧气缓缓挤入烧瓶,铜片慢慢消失.(1)请写出上述过程A装置中所涉及的化学反应方程式.
Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
| ||
Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
;
| ||
2Cu+2H2SO4+O2
2CuSO4+2H2O或2Cu+O2
2CuO,CuO+H2SO4═CuSO4+2H2O
| ||
| ||
2Cu+2H2SO4+O2
2CuSO4+2H2O或2Cu+O2
2CuO,CuO+H2SO4═CuSO4+2H2O
| ||
| ||
(2)张老师认为实验中B装置设计有误,请你帮助小明在答题卡上的对应装置中进行修改

(3)B中所收集到的气体既具有氧化性又具有还原性,请写出一个体现其还原性的化学方程式:
2SO2+O2
2SO3
| ||
| △ |
2SO2+O2
2SO3
,为了验证其漂白性,还可将其通入
| ||
| △ |
品红
品红
试液进行观察.(4)装置C中的应盛放的试剂为
NaOH
NaOH
.分析:(1)依据装置图和实验步骤分析,装置A中在关闭a后加热烧瓶反应,铜和浓硫酸反应生成硫酸铜、二氧化硫和水,再打开活塞a,将气球中的氧气缓缓挤入烧瓶,铜片慢慢消失是铜和氧气反应生成氧化铜,氧化铜和硫酸反应生成硫酸铜和水;
(2)B装置是收集装置,二氧化硫气体比空气重,需要用向上排气法收集;
(3)二氧化硫气体的氧化性是硫元素化合价降低,表现还原性是硫元素化合价升高分析,二氧化硫的漂白性用品红试液验证;
(4)二氧化硫是污染性的气体,不能排放到空气中,需要用氢氧化钠溶液吸收.
(2)B装置是收集装置,二氧化硫气体比空气重,需要用向上排气法收集;
(3)二氧化硫气体的氧化性是硫元素化合价降低,表现还原性是硫元素化合价升高分析,二氧化硫的漂白性用品红试液验证;
(4)二氧化硫是污染性的气体,不能排放到空气中,需要用氢氧化钠溶液吸收.
解答:解:(1)装置图和实验步骤可知,先关闭活塞a,加热至烧杯中不再有气泡产生时,停止反应,此时烧瓶中铜片仍有剩余,此时反应为Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O;再打开活塞a,将气球中的氧气缓缓挤入烧瓶,铜片慢慢消失,发生的反应为:2Cu+2H2SO4+O2
2CuSO4+2H2O;或2Cu+O2
2CuO,CuO+H2SO4═CuSO4+2H2O,
故答案为:Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O;2Cu+2H2SO4+O2
2CuSO4+2H2O;或2Cu+O2
2CuO,CuO+H2SO4═CuSO4+2H2O;
(2)B装置是收集装置,二氧化硫气体比空气重,需要用向上排气法收集,导气管长进短出,装置为: ,故答案为:
,故答案为: ;
;
(3)二氧化硫气体的氧化性是硫元素化合价降低,表现还原性是硫元素化合价升高的反应,如:2SO2+O2
2SO3;二氧化硫的漂白性用品红试液验证,
故答案为:2SO2+O2
2SO3;品红;
(4)二氧化硫是污染性的气体,不能排放到空气中,需要用氢氧化钠溶液吸收,故答案为:NaOH.
| ||
| ||
| ||
故答案为:Cu+2H2SO4(浓)
| ||
| ||
| ||
(2)B装置是收集装置,二氧化硫气体比空气重,需要用向上排气法收集,导气管长进短出,装置为:
 ,故答案为:
,故答案为: ;
;(3)二氧化硫气体的氧化性是硫元素化合价降低,表现还原性是硫元素化合价升高的反应,如:2SO2+O2
| ||
| △ |
故答案为:2SO2+O2
| ||
| △ |
(4)二氧化硫是污染性的气体,不能排放到空气中,需要用氢氧化钠溶液吸收,故答案为:NaOH.
点评:本题考查了浓硫酸的性质实验验证,产物性质的实验验证,注意尾气吸收装置和收集装置的分析判断,题目难度中等.

练习册系列答案
相关题目
 I.小明对妈妈杀鱼时从鱼肚内取出的鳔(见图)产生了兴趣.他拟定“探究鳔内气体体积和成分”作为研究性学习的课题.小明通过查阅有关资料获知:这种鱼鳔内氧气约占四分之一其余主要为二氧化碳和氮气.探究分两步进行.
I.小明对妈妈杀鱼时从鱼肚内取出的鳔(见图)产生了兴趣.他拟定“探究鳔内气体体积和成分”作为研究性学习的课题.小明通过查阅有关资料获知:这种鱼鳔内氧气约占四分之一其余主要为二氧化碳和氮气.探究分两步进行.