题目内容
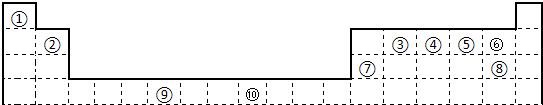
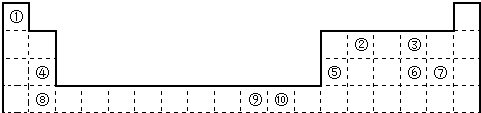
下表为长式周期表的一部分,其中的编号代表对应的元素.
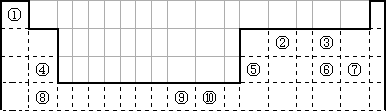
请回答下列问题:
(1)表中属于S区的元素是________(填编号).
(2)写由上述元素组成的分子中电子总数为10的两种分子:________.
(3)元素①与②组成的化合物中,有一种含6原子分子是重要的化工原料,常把该物质作为衡量石油化工发展水平的标志.有关该氢化物分子的说法正确的是________.
A.属于含有极性键的极性分子
B.只含有4个sp-s的σ键和1个p-p的π键
C.该分子中②原子采用sp2杂化
(4)某元素的价电子排布式为nsnnpn+1,该元素原子的核外最外层电子的孤对电子数为________;该元素与元素①形成的10电子的分子的电子式为________;
(5)下表为原子序数依次增大的短周期元素A~F的第一到第五电离能数据.
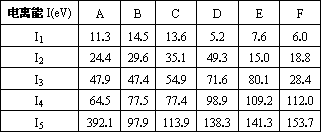
请回答:表中的非金属元素是________(填字母);若E、F为原子序数依次增大的同周期相邻元素,表中显示E比F的第一电离能略大,其原因是________________.
答案:
解析:
解析:
|
(1)①④⑧ (2)CH4、H2O (3)C (4)1 (5)A、B、C;(填对任意2个就给2分) E的nS轨道上的电子全充满,能量比F低,自身更稳定,所以第一电离能比F大 |

练习册系列答案
相关题目