题目内容
下列根据实验操作和现象所得出的结论不正确的是
选项 实验操作 实验现象 结论
A 向硅酸钠溶液中滴加1滴酚酞,然后逐滴加入稀盐酸至红色褪去 2min后,试管里出现凝胶 酸性:盐酸>硅酸
B 在酒精灯上加热铝箔 铝箔熔化但不滴落 熔点:氧化铝>铝
C 常温下,向浓硫酸中投入铁片 铁片不溶解 常温下,铁不与浓硫酸反应
D 向某溶液中先滴加KSCN溶液,再滴加少量氯水 先无明显现象,后溶液变成血红色 溶液中含有Fe2+,没有Fe3+
C
【解析】
试题分析:A、向硅酸钠溶液中滴加1滴酚酞,然后逐滴加入稀盐酸至红色褪去,2min后出现凝胶。这说明反应中有硅酸生成。因此根据较强的酸制备较弱的酸可知,盐酸的酸性强于硅酸的酸性,A正确;B、铝是活泼的金属,其表面有一层氧化铝薄膜。在酒精灯上加热铝箔,铝箔熔化但不滴落,这说明熔点:氧化铝>铝,B正确;C、常温下,铁与浓硫酸发生钝化,但钝化是化学变化,所以常温下铁能和浓硫酸反应。看不见现象,是由于表面生成了一层致密的氧化膜,阻止了反应继续进行,C不正确;D、向某溶液中先滴加KSCN溶液,无明显现象,说明没有铁离子。再滴加少量氯水后溶液变成血红色,说明溶液中含有亚铁离子,被氯水氧化生成了铁离子与KSCN溶液反应而变红色,D正确,答案选C。
考点:考查实验方案的设计与评价

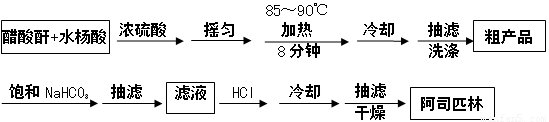
阿司匹林是一种历史悠久的解热镇痛药,学名为乙酰水杨酸,结构简式为 。某探究小组在实验室探究阿司匹林的合成,主要原料是水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O],制备基本实验流程如下:
。某探究小组在实验室探究阿司匹林的合成,主要原料是水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O],制备基本实验流程如下:
已知:1、乙酰水杨酸是白色晶体,易溶于乙醇、乙醚,在128~135℃易分解。
2、主要试剂和产品的其它物理常数
|
名称 |
相对分子质量 |
熔点或沸点(℃) |
水溶性 |
|
水杨酸 |
132 |
158(熔点) |
微溶 |
|
醋酸酐 |
102 |
139.4(沸点) |
与水反应 |
|
乙酰水杨酸 |
180 |
135(熔点) |
微溶 |
请根据以上信息回答下列问题:
(1)写出水杨酸与醋酸酐制备阿司匹林的化学方程式 。
(2)制备阿司匹林主反应时,仪器必须干燥的原因是 。
(3)合成阿司匹林主反应时,最合适的加热方法是 ,除酒精灯外,该加热装置还需要的玻璃仪器有 。
(4)提纯粗产品时加入饱和NaHCO3溶液至没有CO2产生为止,再抽滤(即减压过滤),结合提纯流程回答加饱和NaHCO3溶液的目的是 。
(5)最终所得产品可能仍含有少量水杨酸,检验含有水杨酸的操作和现象是
。



