题目内容
【题目】过渡态理论认为:化学反应并不是通过简单的碰撞就能完成的,而是从反应物到生成物的过程中经过一个高能量的过渡态.如图I是1molNO2与1molCO恰好反应生成CO2和NO过程中的能量变化示意图。
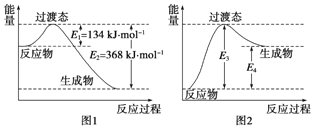
(1)试写出NO2 和CO反应的热化学方程式:____.该反应的活化能是___kJ·mol-1
(2) 图2 是某学生模仿图l画出的NO(g)+CO2(g)= NO2(g)十CO(g)的能量变化示意图。则图中E3=_kJ·mol-1,E4=____ kJ·mol-1
【答案】(1)NO2(g)+CO(g)= NO(g)+CO2(g) ΔH=-234 kJ·mol-1;134;(2)368;234。
【解析】
试题分析:(1)根据图示可知反应物的能量高于生成物的能量,所以该反应是放热反应,反应热是△H= —(368kJ/mol-134kJ/mol)= -234 kJ/mol,所以该反应的热化学方程式是:NO2(g)+CO(g)= NO(g)+CO2(g) ΔH=-234 kJ·mol-1;活化能是反应物具有的能量与该反应发生所需要的最低能量的差值,根据图示可知该反应的活化能是134kJ·mol-1;(2)根据图示可知。该图像是图1反应的逆反应,则该反应的E3是该反应的活化能,在数值上等于图1 的E2,是E3=368kJ/mol;E4的图1中反应的活化能,E4=134 kJ/mol。

练习册系列答案
相关题目

