题目内容
某高二化学兴趣小组为了探索铝电极在原电池中的作用,设计并进行了以下一系列实验,实验结果记录如下:
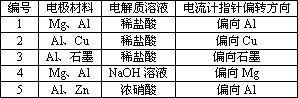
根据上表中的实验现象完成下列问题:
(1)实验1、2中Al所作的电极是否相同?________.
(2)写出实验3中的正极、负极电极反应式和电池总反应方程式.
铝为(________极)________;石墨为(________极)________.
电池总反应:________.
(3)实验4中的铝作正极还是负极?________,为什么?________.
写出铝电极的电极反应式:________.
(4)解释实验5中电流计指针偏向铝的原因:________.
(5)根据实验结果总结:在原电池中金属铝作正极还是作负极受到哪些因素的影响?
解析:
|
答案:(1)不同 (2)负 Al-3e- (3)负极 铝能与NaOH溶液反应 Al+4OH--3e- (4)由于铝在浓硝酸中发生钝化,所以锌为负极 (5)与另一种材料的活泼性、电解质溶液的酸碱性以及电解质溶液的氧化性强弱等因素有关. 思路解析:本题考查知识点是根据氧化还原反应原理来设计原电池.实验1中Mg活泼,故Mg作负极;实验2中Al活泼,故Al作负极;实验3中铝作负极,将盐酸中的氢离子置换出氢气;实验4中Mg虽比Al活泼,但Mg不能与NaOH溶液反应,而Al可与NaOH溶液反应,故Al作负极;实验5中Al虽比Zn活泼,但常温下,Al遇浓硝酸发生钝化,阻止内部的金属继续与酸反应,故Zn为负极. |
提示:
|
设计原电池时,将相对金属性较强的金属作负极,将相对金属性较弱的金属作正极;负极发生氧化反应,正极发生还原反应. |

编号 | 电极材料 | 电解质溶液 | 电流计指针偏转方向 |
1 | Mg、Al | 稀盐酸 | 偏向Al |
2 | Al、Cu | 稀盐酸 | 偏向Cu |
3 | Al、石墨 | 稀盐酸 | 偏向石墨 |
4 | Mg、Al | NaOH溶液 | 偏向Mg |
5 | Al、Zn | 浓硝酸 | 偏向Al |
根据上表中的实验现象完成下列问题:
(1)实验1、2中Al所作的电极是否相同?________________。
(2)写出实验3中的正极、负极电极反应式和电池总反应方程式。
铝为(__________极)__________;石墨为(__________极)__________。
电池总反应: _____________________________________________________。
(3)实验4中的铝作正极还是负极?__________,为什么?______________________________。
写出铝电极的电极反应式:______________________________________________。
(4)解释实验5中电流计指针偏向铝的原因: __________________________________________。
(5)根据实验结果总结:在原电池中金属铝作正极还是作负极受到哪些因素的影响?
编号 | 电极材料 | 电解质溶液 | 电流计指针偏转方向 |
1 | Mg、Al | 稀盐酸 | 偏向Al |
2 | Al、Cu | 稀盐酸 | 偏向Cu |
3 | Al、石墨 | 稀盐酸 | 偏向石墨 |
4 | Mg、Al | NaOH溶液 | 偏向Mg |
5 | Al、Zn | 浓硝酸 | 偏向Al |
根据上表中的实验现象完成下列问题:
(1)实验1、2中Al所作的电极是否相同?________________。
(2)写出实验3中的正极、负极电极反应式和电池总反应方程式。
铝为(__________极)__________;石墨为(__________极)__________。
电池总反应: _____________________________________________________。
(3)实验4中的铝作正极还是负极?__________,为什么?______________________________。
写出铝电极的电极反应式:______________________________________________。
(4)解释实验5中电流计指针偏向铝的原因: __________________________________________。
(5)根据实验结果总结:在原电池中金属铝作正极还是作负极受到哪些因素的影响?
 进行了以下一系
进行了以下一系 列实验,实验结果记录如下:
列实验,实验结果记录如下:


