题目内容
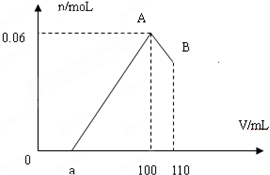 一定质量的镁、铝合金溶于400mL过量的盐酸中,然后在所得溶液中逐滴加入2mol/L氢氧化钠溶液,所得沉淀的物质的量与所加氢氧化钠溶液的体积关系如图:
一定质量的镁、铝合金溶于400mL过量的盐酸中,然后在所得溶液中逐滴加入2mol/L氢氧化钠溶液,所得沉淀的物质的量与所加氢氧化钠溶液的体积关系如图:(1)写出AB段的离子方程式:
(2)盐酸的物质的量浓度为
(3)O点的体积
(4)镁、铝的物质的量之比:
考点:铝的化学性质,化学方程式的有关计算,镁的化学性质
专题:计算题
分析:由图可知,从开始至加入NaOH溶液amL,没有沉淀生成,说明原溶液中盐酸溶解Mg、Al后盐酸有剩余,此时发生的反应为HCl+NaOH═NaCl+H2O;继续滴加NaOH溶液,到氢氧化钠溶液为100mL时,沉淀量最大,镁离子、铝离子与氢氧根反应生成Mg(OH)2和Al(OH)3,溶液为氯化钠溶液;再继续滴加NaOH溶液,氢氧化铝与氢氧化钠反应生成偏铝酸钠与水,发生反应Al(OH)3+NaOH═NaAlO2+2H2O,以此计算解答.
解答:
解:(1)AB段发生Al(OH)3+NaOH═NaAlO2+2H2O,离子方程式为Al(OH)3+OH-═AlO2-+2H2O,故答案为:Al(OH)3+OH-═AlO2-+2H2O;
(2)由图可知,100mL时溶质为NaCl,由原子守恒可知,n(HCl)=n(NaOH)=0.1L×2mol/L=0.2mol,盐酸的物质的量浓度为
=0.5mol/L,故答案为:0.5mol/L;
(3)由100mL~110mL发生Al(OH)3+NaOH═NaAlO2+2H2O可知,n(Al)=n(Al(OH)3)=0.01L×2mol/L=0.02mol,
A点沉淀共0.06mol,则Mg(OH)2的物质的量为0.06mol-0.02mol=0.04mol,n(Mg)=0.04mol,
则Mg~Mg2+~2OH-~Mg(OH)2↓
0.04 0.08
Al~Al3+~3OH-~Al(OH)3↓
0.02 0.06
消耗NaOH的体积为
=0.07L=70mL,
则a为100mL-70mL=30mL,故答案为:30;
(4)由(3)中计算可知,镁、铝的物质的量之比为0.04mol:0.02mol=2:1,故答案为:2:1.
(2)由图可知,100mL时溶质为NaCl,由原子守恒可知,n(HCl)=n(NaOH)=0.1L×2mol/L=0.2mol,盐酸的物质的量浓度为
| 0.2mol |
| 0.4L |
(3)由100mL~110mL发生Al(OH)3+NaOH═NaAlO2+2H2O可知,n(Al)=n(Al(OH)3)=0.01L×2mol/L=0.02mol,
A点沉淀共0.06mol,则Mg(OH)2的物质的量为0.06mol-0.02mol=0.04mol,n(Mg)=0.04mol,
则Mg~Mg2+~2OH-~Mg(OH)2↓
0.04 0.08
Al~Al3+~3OH-~Al(OH)3↓
0.02 0.06
消耗NaOH的体积为
| 0.08mol+0.06mol |
| 2mol/L |
则a为100mL-70mL=30mL,故答案为:30;
(4)由(3)中计算可知,镁、铝的物质的量之比为0.04mol:0.02mol=2:1,故答案为:2:1.
点评:本题以图象题的形式考查镁铝化合物性质、混合物的计算,题目难度中等,分析图象各阶段的发生的反应是解题关键,注意利用守恒思想进行计算.

练习册系列答案
相关题目
现代建筑门框架,常用电解加工成古铜色的硬铝制造.硬铝是( )
| A、Al-Mg合金 |
| B、Al-Cu-Mg-Mn-Si合金 |
| C、Al-Si合金 |
| D、表面的氧化铝膜的纯铝 |
 科学家已获得了极具理论研究意义的N4分子,其结构为正四面体(如图所示),与白磷分子相似.已知断裂1molN-N键吸收193kJ热量,断裂1molN≡N键吸收941kJ热量,则1molN4气体转化为2molN2时要放出
科学家已获得了极具理论研究意义的N4分子,其结构为正四面体(如图所示),与白磷分子相似.已知断裂1molN-N键吸收193kJ热量,断裂1molN≡N键吸收941kJ热量,则1molN4气体转化为2molN2时要放出