题目内容
| A、d=a+17b | ||
B、C1=
| ||
C、铝为
| ||
| D、与金属反应后剩余盐酸为(C1V1-b)mol |
A.根据电荷守恒可知,金属提供电子物质的量等于沉淀中氢氧根离子的物质的量,根据电子转移计算金属提供的电子,沉淀质量=m(金属)+m(沉淀中氢氧根);
B.反应后溶液的成分为NaCl,根据原子守恒可知n(HCl)=n(NaCl)=n(NaOH),据此计算;
C.设合金中含有xmolMg,ymolAl,根据生成氢气的物质的量和金属的质量可列方程组计算合金中镁和铝的物质的量;
D.总盐酸的物质的量减去生成氢气所用盐酸的物质的量即为剩余盐酸的物质的量.
A.根据电子转移守恒可知,金属提供的电子物质的量为
| bg |
| 2g/mol |
B.反应后溶液的成分为NaCl,根据原子守恒可知n(HCl)=n(NaCl)=n(NaOH),则C1×V1=C2×V2,故C1=
| C2V2 |
| V1 |
C.设合金中含有xmolMg,ymolAl,反应的化学方程式分别为:Mg+2HCl═MgCl2+H2↑,2Al+6HCl═2AlCl3+3H2↑,产生bg H2,
|
|
D、生成bgH2,其物质的量为0.5b mol,根据氢元素守恒,可知消耗盐酸bmol,则剩余HCl为(c1V1-b)mol,故D正确;
故选C.

(17分)蛇纹石可以看作由MgO、Fe2O3、Al2O3、SiO2组成。实验室以蛇纹石为原料制取水合碱式碳酸镁,已知:
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀pH | 1.5 | 3.3 | 9.4 |
实验步骤如下:
请回答下列问题:
(1)实验室完成操作①所用到的玻璃仪器有________________ 。
(2)检验溶液Ⅱ中是否含有Fe3+的操作与结论是___________________________
_____________________________________________________________________。
(3)从沉淀混合物B中制取D,应加入一种试剂进行分离,其反应的离子方程式为________________________________________________________________________,
再进行__________、 、 (依次填写实验操作名称)。
(4)操作②中应控制溶液pH的合理范围是____(填序号)。
A.小于1.5 B.1.5~3.3
C.7~8 D.大于9.4
(5)为探究所得的水合碱式碳酸镁[xMgCO3·yMg(OH)2·zH2O]的组成,取样7.28 g于装置A的玻璃管中,请按由左―→右顺序将下列装置连接好(填序号,装置可重复使用):________________________________________________________________________,
装置C应盛的试剂是______________________。
(17分)蛇纹石可以看作由MgO、Fe2O3、Al2O3、SiO2组成。实验室以蛇纹石为原料制取水合碱式碳酸镁,已知:
|
氢氧化物 |
Fe(OH)3 |
Al(OH)3 |
Mg(OH)2 |
|
开始沉淀pH |
1.5 |
3.3 |
9.4 |
实验步骤如下:

请回答下列问题:
(1)实验室完成操作①所用到的玻璃仪器有________________ 。
(2)检验溶液Ⅱ中是否含有Fe3+的操作与结论是___________________________
_____________________________________________________________________。
(3)从沉淀混合物B中制取D,应加入一种试剂进行分离,其反应的离子方程式为________________________________________________________________________,
再进行__________、 、 (依次填写实验操作名称)。
(4)操作②中应控制溶液pH的合理范围是____(填序号)。
A.小于1.5 B.1.5~3.3
C.7~8 D.大于9.4
(5)为探究所得的水合碱式碳酸镁[xMgCO3·yMg(OH)2·zH2O]的组成,取样7.28 g于装置A的玻璃管中,请按由左―→右顺序将下列装置连接好(填序号,装置可重复使用):________________________________________________________________________,

装置C应盛的试剂是______________________。
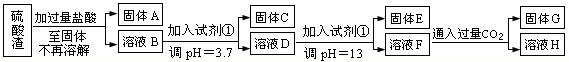
 蛇纹石可以看作由MgO、Fe2O3、Al2O3、SiO2组成.实验室以蛇纹石为原料制取水合碱式碳酸镁,已知:
蛇纹石可以看作由MgO、Fe2O3、Al2O3、SiO2组成.实验室以蛇纹石为原料制取水合碱式碳酸镁,已知: