题目内容
氢氧燃料电池是符合绿色化学理念的新型发电装置.右图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:(1)氢氧燃料电池的能量转化主要形式是 ,在导线中电子流动方向为 (用a、b 表示).
(2)负极反应式为 .
(3)电极表面镀铂粉的原因为 .
(4)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能.因此,大量安全储氢是关键技术之一.金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
Ⅰ.2Li+H2
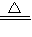 2LIH
2LIHⅡ.LiH+H2O=LiOH+H2↑
反应Ⅰ中的还原剂是 ,反应Ⅱ中的氧化剂是 .
【答案】分析:(1)根据原电池的定义分析;根据得失电子判断;
(2)根据得失电子写出电极反应式;
(3)根据外界条件对化学反应速率的影响因素分析;
(4)根据化合价的变化判断;
解答:解:(1)该装置把化学能转变为电能,所以是原电池;发生反应时,氢气失电子,氧气的电子,所以电子的流动方向是由由a到b.
故答案为:由化学能转变为电能;由a到b.
(2)负极上氢气失电子和氢氧根离子生成水,所以电极反应式为 H2+2OH--2e-=2H2O.
故答案为:H2+2OH--2e-=2H2O.
(3)该电池电极表面镀一层细小的铂粉,增大了电极单位面积吸附H2、O2分子数,相当于增大反应物的浓度,所以加快电极反应速率.
故答案为:增大电极单位面积吸附H2、O2分子数,加快电极反应速率.
(4)2Li+H2 2LiH,该反应中锂失电子发生氧化反应,所以锂是还原剂;LiH+H2O=LiOH+H2↑,该反应中H2O得电子生成氢气,发生还原反应,所以H2O是氧化剂.
2LiH,该反应中锂失电子发生氧化反应,所以锂是还原剂;LiH+H2O=LiOH+H2↑,该反应中H2O得电子生成氢气,发生还原反应,所以H2O是氧化剂.
故答案为:Li; H2O.
点评:本题考查了原电池工作原理,写电极反应式要注意结合电解质溶液书写,如果电解质溶液不同,虽然原料相同,电极反应式也不同,如氢氧燃料电池,当电解质为酸或碱,电极反应式就不同.
(2)根据得失电子写出电极反应式;
(3)根据外界条件对化学反应速率的影响因素分析;
(4)根据化合价的变化判断;
解答:解:(1)该装置把化学能转变为电能,所以是原电池;发生反应时,氢气失电子,氧气的电子,所以电子的流动方向是由由a到b.
故答案为:由化学能转变为电能;由a到b.
(2)负极上氢气失电子和氢氧根离子生成水,所以电极反应式为 H2+2OH--2e-=2H2O.
故答案为:H2+2OH--2e-=2H2O.
(3)该电池电极表面镀一层细小的铂粉,增大了电极单位面积吸附H2、O2分子数,相当于增大反应物的浓度,所以加快电极反应速率.
故答案为:增大电极单位面积吸附H2、O2分子数,加快电极反应速率.
(4)2Li+H2
 2LiH,该反应中锂失电子发生氧化反应,所以锂是还原剂;LiH+H2O=LiOH+H2↑,该反应中H2O得电子生成氢气,发生还原反应,所以H2O是氧化剂.
2LiH,该反应中锂失电子发生氧化反应,所以锂是还原剂;LiH+H2O=LiOH+H2↑,该反应中H2O得电子生成氢气,发生还原反应,所以H2O是氧化剂.故答案为:Li; H2O.
点评:本题考查了原电池工作原理,写电极反应式要注意结合电解质溶液书写,如果电解质溶液不同,虽然原料相同,电极反应式也不同,如氢氧燃料电池,当电解质为酸或碱,电极反应式就不同.

练习册系列答案
 金牌课堂练系列答案
金牌课堂练系列答案 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案
相关题目
 AgOH+H+
AgOH+H+
 门上的固体材料R可以采用
门上的固体材料R可以采用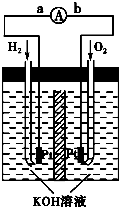 方向为
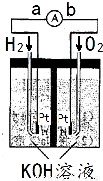
方向为 氢氧燃料电池是符合绿色化学理念的新型发电装置.如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:
氢氧燃料电池是符合绿色化学理念的新型发电装置.如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答: 氢氧燃料电池是符合绿色化学理念的新型发电装置,右图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定.请回答:
氢氧燃料电池是符合绿色化学理念的新型发电装置,右图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定.请回答:
 氢氧燃料电池是符合绿色化学理念的新型 发电装置.如图为电池示意图,该电池电极表面镀一层细小的铂粉,吸附气体的 能力强,性质稳定,请回答:
氢氧燃料电池是符合绿色化学理念的新型 发电装置.如图为电池示意图,该电池电极表面镀一层细小的铂粉,吸附气体的 能力强,性质稳定,请回答: