题目内容
|
将 8.02 g铁片放入1.0 L 0.90 mol/L CuSO4溶液中,过一段时间取出洗净、干燥后称量,质量变为8.66 g.假设溶液的体积无变化,则Cu2+的浓度变为 | |
| [ ] | |
A. |
0.89 mol/L |
B. |
0.82 mol/L |
C. |
0.78 mol/L |
D. |
0.60 mol/L |
答案:B
解析:
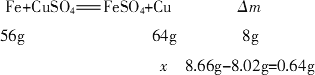
解析:
设反应生成的铜的质量为
x,根据反应方程式: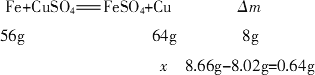
解得
x=5.12 g,故析出铜的物质的量:n(Cu)=0.08 mol,原溶液中剩余的Cu2+的物质的量为0.90 mol-0.08 mol=0.82 mol,溶液体积不变时,Cu2+的浓度为0.82 mol/L.
练习册系列答案
相关题目
 2C(g)
2C(g) :
: aA (g)+ bB (g)
aA (g)+ bB (g)  2C(g)
2C(g) 
 2C(g)
2C(g)