题目内容
当把晶体N2O4放入密闭容器中气化,并建立了N2O4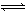 2NO2平衡后,保持温度不变,再通入若干N2O4气体,待反应达到新的平衡时,则新平衡与旧平衡相比,其
2NO2平衡后,保持温度不变,再通入若干N2O4气体,待反应达到新的平衡时,则新平衡与旧平衡相比,其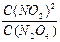 比值
比值
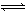 2NO2平衡后,保持温度不变,再通入若干N2O4气体,待反应达到新的平衡时,则新平衡与旧平衡相比,其
2NO2平衡后,保持温度不变,再通入若干N2O4气体,待反应达到新的平衡时,则新平衡与旧平衡相比,其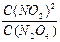 比值
比值| A.变大 | B.不变 | C.变小 | D.无法确定 |
B
略

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
题目内容
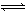 2NO2平衡后,保持温度不变,再通入若干N2O4气体,待反应达到新的平衡时,则新平衡与旧平衡相比,其
2NO2平衡后,保持温度不变,再通入若干N2O4气体,待反应达到新的平衡时,则新平衡与旧平衡相比,其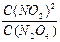 比值
比值| A.变大 | B.不变 | C.变小 | D.无法确定 |

 阅读快车系列答案
阅读快车系列答案