题目内容
某兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如图所示:

(1)下列实验方案适用于在实验室制取所需SO2的是 ;
A.Na2SO3溶液与HNO3 B.Na2SO3固体与浓硫酸
C.固体硫在纯氧中燃烧 D.碳与热浓H2SO4
(2)装置C的作用是
(3)写出SO2气体通入A中的离子反应方程式_________________________________________;
(4)在上述装置中通入过量的SO2,为了验证A中SO2与Fe3+发生了氧化还原反应,
取A中的溶液,分成两份,并设计了如下实验:
方案①:往第一份试液中加入少量酸性KMnO4溶液,紫红色褪去
方案②:往第二份试液加入KSCN溶液,不变红,再加入新制的氯水,溶液变红
上述方案不合理的是 ,原因是 ;
⑸能表明I−的还原性弱于SO2的现象是 。
⑴ B ;
⑵ 吸收未反应的SO2 防止空气污染 ;
⑶ SO2 +2Fe3+ +2H2O== 2Fe2+ + SO42-+ 4H+ ;
⑷上述方案不合理的是 1 ,原因是 过量的 SO2 也能使酸性高锰酸钾溶液褪色 ;
⑸ 装置B中溶液蓝色退去 。

 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案
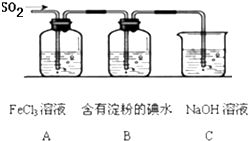 某兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如图所示:
某兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如图所示:

