题目内容
16.今有CH4、C2H2、C2H4、C2H6、C3H6五种链状有机物.相同状况下,同质量时体积最大的是CH4,完全燃烧生成二氧化碳最多的是C2H2;相同状况下,同体积的这五种气体完全燃烧时耗氧量最多的是C3H6;二氯代物有两种的饱和烃是C2H6.分析 根据n=$\frac{m}{M}$可知,相同质量情况下,摩尔质量越小,物质的量越大,相同条件下,体积之比等于物质的量之比;
相同质量情况下,碳元素质量分数越大,完全燃烧生成二氧化碳越多;
同状况同体积时,气体的物质的量相等,1mol烃的耗氧量为(x+$\frac{y}{4}$)mol,据此计算判断;
利用定一移二法确定二氯代物的同分异构体数目,写出一氯代物,再根据分子中含有H原子种类,判断二氯代物的数目.
解答 解:CH4、C2H2、C2H4、C2H6、C3H6的摩尔质量依次增大,根据n=$\frac{m}{M}$可知,相同质量情况下,摩尔质量越小,物质的量越大,相同条件下,体积之比等于物质的量之比,故甲烷的体积最大;
同质量时,C元素质量分数越大,生成二氧化碳越多,H元素质量分数越大,生成水的量越多,CH4、C2H2、C2H4、C2H6、C3H6分子中C、H原子数目之比分别为:1:4、1:1、1:2、1:3、1:2,故C2H2中碳元素质量分数最大,故C2H2生成二氧化碳最多;
同状况同体积时,气体的物质的量相等,1mol烃的耗氧量为(x+$\frac{y}{4}$)mol,1molCH4、C2H2、C2H4、C2H6、C3H6耗氧量分别为2mol、2.5mol、3mol、3.5mol、4.5mol,故C3H6耗氧量最多;
五种链状有机物中属于饱和烃的是CH4、C2H6、C3H6,CH4为正四面体二氯代物只有一种,C2H6的二氯代物有两种为CH3CH(Cl)2和CH2ClCH2Cl,CH3CH2CH2Cl中含有3种H原子,再次一氯取代有3种产物,CH3CH(Cl)CH3中含有2种H原子,再次一氯取代有2种产物,其中有两种为同一物质,故丙烷的二氯代物有4种;
故答案为:CH4;C2H2;C3H6;C2H6.
点评 本题考查烃燃烧有关计算问题,题目难度中等,注意根据燃烧通式判断耗氧量问题,注意对规律的归纳总结.

(1)下面表格中的数据(铁和铜的某些物理数据)摘自某化学手册.
| 金属 | 颜色 | 密度(g/cm3) | 熔点(℃) | 沸点(℃) | 比热[KJ/kg•℃] |
| Fe | 银白色 | 7.86 | 1 535 | 2 750 | 0.44 |
| Cu | 红色 | 8.92 | 1 083 | 2 567 | 0.38 |
(2)考古中出土的青铜器、铁剑等往往锈迹斑斑.请完成下面铜、铁制品在自然条件下发生锈蚀的化学方程式:
①□Cu+□O2+□H2O+□CO2═□Cu2(OH)2CO3
②□Fe+□O2+□H2O═□Fe2O3•nH2O
(3)镁、铝是现代人常用的金属材料,这些活泼金属的冶炼方法是电解法,工业生产中,镁的冶炼采用的反应物是熔融氯化镁(或MgCl2),铝的冶炼采用的反应物是熔融氧化铝(或Al2O3).
(1)科学家一直致力于“人工固氮”的新方法研究.据报道,在光照条件下,N2在催化剂表面与水发生反应生成NH3和另一种单质.在使用催化剂和不使用催化剂时,该反应过程和能量的变化关系如图所示.
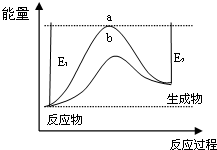
①写出该反应的化学方程式2N2+6H2O$\frac{\underline{\;催化剂\;}}{光照}$4NH3+3O2.
②a和b相比,二者的平衡常数关系是Ka=Kb(填“>”、“=”或“<”).
③升高温度,平衡时NH3的含量增大(填“增大”、“不变”或“减小”).
(2)在 0.5L的密闭容器中,一定量的 N2和H2发生反应:N2(g)+3H2(g)?2NH3(g)△H<0,
400℃时,K=0.5,某一时刻测得N2、H2 和NH3三种物质物质的量分别为2mol、2mol和3mol,则该反应的v正(N2)>v逆(N2)(填“>”“=”或“<”).
(3)将NH3气体通入稀盐酸中,若存在[NH4+]>[Cl-]>[OH-]>[H+]的关系,此时所得溶液的溶质是NH3.H2O、NH4Cl(填化学式).
(4)NH3的催化氧化反应是工业制HNO3的关键步骤,测得某温度下固定容积的容器中的数据为:
| 浓度/mol•L-1 时间 | c(NH3) | c(O2) | c(NO) |
| 0min | 1.000 | 1.600 | 0.000 |
| 2min | 0.600 | a | 0.400 |
| 4min | 0.500 | 0.975 | 0.500 |
| 6min | 0.500 | 0.975 | 0.500 |
| 8min | 0.700 | 1.225 | 0.750 |
②在第8min时改变条件,你认为改变的条件可能是增大NO的浓度.
| A. | 第5周期第IA族 | B. | 第4周期第IA族 | C. | 第3周期第IA族 | D. | 第3周期第IA族 |
| A. | 甲烷与氯气反应:CH4+4Cl2→CCl4+4HCl | |
| B. | 用醋酸除去水垢:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| C. | 乙醇和钠反应:2CH3CH2OH+2Na→2CH3CH2ONa+H2↑ | |
| D. | 苯和浓硝酸、浓硫酸的混合物水浴60℃反应: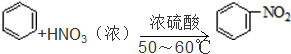 |
| A. | 聚二氧化碳塑料是通过加聚反应制得的 | |
| B. | 聚二氧化碳塑料与干冰互为同素异形体 | |
| C. | 聚二氧化碳塑料与干冰都属于纯净物 | |
| D. | 聚二氧化碳塑料的使用会产生白色污染 |
| A. | CH4$\stackrel{高温}{→}$C+2H2 | |
| B. | CH3CH=CH2+Br2$\stackrel{CCl_{4}}{→}$CH3CHBrCH2Br | |
| C. | CH4+2O2$\stackrel{点燃}{→}$CO2+2H2O | |
| D. | C2H6+Cl2$\stackrel{光}{→}$C2H5Cl+HCl |
| A. | 氧化铜(铜) | B. | 碳酸钙(氯化银) | C. | 氢氧化铁(氯化铁) | D. | 氢氧化钠(氯化钠) |
| A. | 分子中键的极性越强,分子越稳定 | |
| B. | 分子中共价键的键能越大,该物质的性质越不活泼 | |
| C. | 分子中共价键的键能越大,键越长,则分子越稳定 | |
| D. | 若把H2S写成H3S,违背了共价键的饱和性 |