题目内容
某学生为了测定部分变质的Na2SO3样品的纯度,设计了如下实验:
回答下列问题:
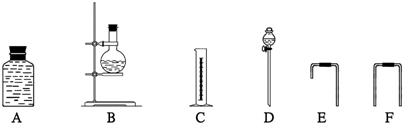
(1)写出A装置中玻璃仪器的名称:酒精灯、_____________、_____________。
(2)写出D中的化学方程式: ;实验开始后,写出B中反应的离子方程式_____。
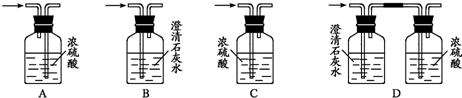
(3)C中的现象是______,E装置的作用是____________________________。
(4)称取25.2g的Na2SO3样品放入A装置的烧瓶中,滴入足量的H2SO4完全反应。然后将B中完全反应后的溶液与足量的BaCl2溶液反应,过滤、洗涤、干燥,得白色沉淀23.3g,则原样品中Na2SO3的纯度为________%
(5)要使测定结果准确应先点燃______处酒精灯(填装置字母)待看到出现 现象时,再通入______
(10分)(1)圆底烧瓶(1分)、分液漏斗(1分),
MnO2+4HCl(浓) =MnCl2↑+Cl2↑+2H2O↑(1分)
SO2+ Cl2 + 2H2O=SO4 2-+ 4H++ 2Cl-(1分),(3)鲜花褪色(1分);吸收多余氯气防污染(1分)50%(1分)D;(1分)黄绿色(1分)SO2(1分)
解析:

练习册系列答案
相关题目