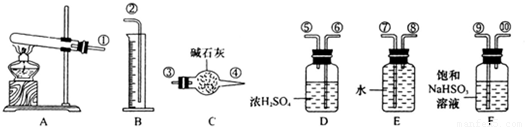
题目内容
 500℃下发生如下反应H2(g)+CO2(g)?H2O(g)+CO(g)△H<0,在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如表所示.(已知此温度下该反应的平衡常数K=
500℃下发生如下反应H2(g)+CO2(g)?H2O(g)+CO(g)△H<0,在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如表所示.(已知此温度下该反应的平衡常数K=| 9 |
| 4 |
| 起始浓度 | 甲 | 乙 | 丙 |
| c(H2)/mol/L | 0.010 | 0.020 | 0.020 |
| c(CO2)/mol/L | 0.010 | 0.010 | 0.020 |
(2)丙中达平衡需要20s,则反应速率v(CO2)=
(3)甲中的反应速率-时间图象如图,在图中画出丙的反应速率-时间图象.
(4)升高温度,平衡常数K
| 9 |
| 4 |
(2)根据甲和丙为等效平衡,二氧化碳的转化率与甲的相等,根据二氧化碳的转化率计算出二氧化碳的反应速率;
(3)根据丙中反应物浓度可知,丙的正逆反应速率都比甲的反应速率大;
(4)根据该反应△H<0,温度升高,平衡向着逆向移动.
H2(g)+CO2(g)?H2O(g)+CO(g)
反应前 0.01mol 0.010mol 0 0
转化 0.01xmol 0.01xmol 0.01xmol 0.01xmol
平衡 0.01-0.01x 0.01-0.01x 0.01xmol 0.01xmol
化学平衡常数为:K=
| 0.01x×0.01x |
| (0.01-0.01x)?(0.01-0.01x) |
| 9 |
| 4 |
解得x=3(舍弃)或x=60%;
反应H2(g)+CO2(g)?H2O(g)+CO(g)中,方程式两边化学计量数之和相等,压强不影响化学平衡,所以甲和丙的转化率相等,由于乙中氢气物质的量浓度比甲的氢气浓度大,所以乙中二氧化碳的转化率大于甲的,甲、乙、丙三个恒容密闭容器中CO2转化率大小关系为:乙>丙=甲,
故答案为:60%;乙>丙=甲;
(2)根据反应H2(g)+CO2(g)?H2O(g)+CO(g)可知,甲和丙为等效平衡,二氧化碳的转化率相同,
所以反应消耗的二氧化碳的浓度为:0.020mol/L×60%=0.012mol/L,
丙中达平衡需要20s,
则反应速率v(CO2)=
| 0.012mol/L |
| 20s |
故答案为:0.0006mol/(L?s);
(3)由于丙中二氧化碳与氢气的浓度都大于甲的,所以反应过程中正逆反应速率都大于甲的反应速率,且达到平衡时丙的反应速率大于甲的,据此画出图象为:
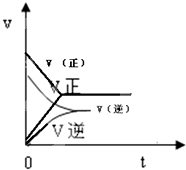
故答案为:

(4)反应H2(g)+CO2(g)?H2O(g)+CO(g)△H<0,温度升高,平衡向着逆向移动,水蒸气、一氧化碳浓度减小,氢气、二氧化碳浓度减小,所以化学平衡常数减小,
故答案为:<.

 提分百分百检测卷系列答案
提分百分百检测卷系列答案化工行业的发展必须符合国家节能减排的总体要求。请回答下列问题:
(1)已知C(s)+H2O(g) CO(g)+H2(g),则该反应的平衡常数表达式为 。
CO(g)+H2(g),则该反应的平衡常数表达式为 。
(2)已知在一定温度下,
C(s)+CO2(g)
 2CO(g)
△H1
2CO(g)
△H1
CO(g)+H2O(g)
 H2(g)+CO2(g)
△H2
H2(g)+CO2(g)
△H2
C(s)+H2O(g) CO(g)+H2(g) △H3
CO(g)+H2(g) △H3
则△H1、△H2、△H3之间的关系是: 。
(3)通过研究不同温度下平衡常数可以解决某些实际问题。已知等体积的一氧化碳和水蒸气进入反应时,会发生如下反应: CO(g)+H2O(g)  H2(g)+CO2(g),该反应平衡常数随温度的变化如表所示。
H2(g)+CO2(g),该反应平衡常数随温度的变化如表所示。
|
温度/℃ |
400 |
500 |
800 |
|
平衡常数K |
9.94 |
9 |
1 |
则该反应的正反应方向是 反应(填“吸热”或“放热”),在500℃时,若设起始时CO和H2O的起始浓度均为0.020mol/L,则CO的平衡转化率为 。
(4)从氨催化氧化可以制硝酸,此过程中涉及氮氧化物,如NO、NO2、N2O4等。对反应N2O4(g)  2NO2(g)
△H>0在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是 :
2NO2(g)
△H>0在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是 :

A.A、C两点的反应速率:A>C
B.A、C两点气体的颜色:A深,C浅
C.B、C两点的气体的平均相对分子质量:B<C
D.由状态A到状态B,可以用加热的方法
E.A、C两点的化学平衡常数:A=C
(5)工业上用Na2SO3吸收尾气中的SO2,再用下图装置电解(惰性电极)NaHSO3制取H2SO4(阴离子交换膜只永许阴离子通过),阳极电极反应式为: ,阳极区逸出气体的成分为 (填化学式)。




 CuO
CuO CuSO4
CuSO4  CuSO4
CuSO4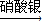 Cu(NO3)2
Cu(NO3)2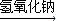 Cu(OH)2
Cu(OH)2 CuSO4
CuSO4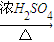 CuSO4
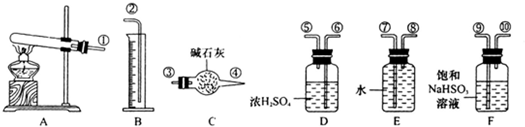
CuSO4 CuO+SO2↑+SO3↑+O2↑,便决定设计试验测定反应生成的SO2、SO3和O2的物质的量,并经计算确定该条件下CuSO4分解反应方程式中各物质的化学计量数.试验可能用到的仪器如下图所示:
CuO+SO2↑+SO3↑+O2↑,便决定设计试验测定反应生成的SO2、SO3和O2的物质的量,并经计算确定该条件下CuSO4分解反应方程式中各物质的化学计量数.试验可能用到的仪器如下图所示: