题目内容
(2009?滨州模拟)Ⅰ.化学兴趣小组对用铜制取硫酸铜晶体的试验方案作研究.甲组同学将铜粉投入盛有稀硫酸的容器中,不发生反应.他们向容器底部缓缓鼓入氧气,溶液慢慢变蓝色,若在溶液中放置有些铂丝,反应速率明显加快.此时,其他组的同学提出方案如下:
乙组:Cu
CuO
CuSO4
丙组:Cu
CuSO4
丁组:Cu
Cu(NO3)2
Cu(OH)2
CuSO4
戊组:Cu
CuSO4
(1)甲组试验可用一个化学反应方程式表示为
(2)可持续发展的原则要求化工生产①原理科学;②能量消耗低;③原料利用率高;④无污染.则在五组方案中,有科学性错误的是
Ⅱ.另一化学兴趣小组从化学手册上查得硫酸铜500℃在以上按照下式分解:
CuSO4
CuO+SO2↑+SO3↑+O2↑,便决定设计试验测定反应生成的SO2、SO3和O2的物质的量,并经计算确定该条件下CuSO4分解反应方程式中各物质的化学计量数.试验可能用到的仪器如下图所示:
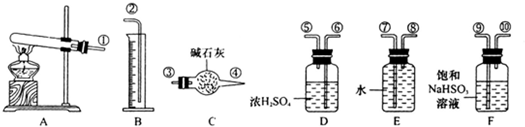
试验测得数据及有关结果如下;
①准确称取6.0g无水CuSO4;②在试验结束时干燥管总质量增加2.4g;③测得量筒中水的体积,得出气体在标准状况下的体积为280mL;试验结束时,装置F中的溶液只含NaHSO4和NaHSO3.按装置从左到右的方向,各仪器接口连结顺序为:①⑨⑩⑥⑤③④⑧⑦②
试回答下列问题:
(1)装置F的作用是
(2)装置D的作用是
(3)为减少测量气体体积引起的误差,应注意的事项有:
①装置内气体的温度应恢复到室温.
②
③
(4)通过计算,推断出该条件下反应的化学方程式
乙组:Cu
| 氧气 |
| △ |
| 稀H2SO4 |
丙组:Cu
| 硫酸亚铁 |
丁组:Cu
| 硝酸银 |
| 氢氧化钠 |
| 稀硫酸 |
戊组:Cu
| 浓H2SO4 |
| △ |
(1)甲组试验可用一个化学反应方程式表示为
2Cu+O2+2H2SO4=2CuSO4+2H2O
2Cu+O2+2H2SO4=2CuSO4+2H2O
;使反应变快的可能原因是形成了原电池
形成了原电池
;从该反应器溶液(含有少量H2SO4以抑制水解)中取得产品的试验操作步骤应为加热蒸发;
加热蒸发;
、冷却结晶
冷却结晶
、过滤并洗涤晶体
过滤并洗涤晶体
,取得产品后的残留物质可循环使用.(2)可持续发展的原则要求化工生产①原理科学;②能量消耗低;③原料利用率高;④无污染.则在五组方案中,有科学性错误的是
丙
丙
组方案,有污染的是戊
戊
组方案,无污染但能量消耗较高的是乙
乙
组方案,因此选择甲
甲
组方案最好.Ⅱ.另一化学兴趣小组从化学手册上查得硫酸铜500℃在以上按照下式分解:
CuSO4
| △ |

试验测得数据及有关结果如下;
①准确称取6.0g无水CuSO4;②在试验结束时干燥管总质量增加2.4g;③测得量筒中水的体积,得出气体在标准状况下的体积为280mL;试验结束时,装置F中的溶液只含NaHSO4和NaHSO3.按装置从左到右的方向,各仪器接口连结顺序为:①⑨⑩⑥⑤③④⑧⑦②
试回答下列问题:
(1)装置F的作用是
吸收SO3,放出等物质的量的SO2
吸收SO3,放出等物质的量的SO2
.(2)装置D的作用是
吸收水分,干燥SO2和O2
吸收水分,干燥SO2和O2
.(3)为减少测量气体体积引起的误差,应注意的事项有:
①装置内气体的温度应恢复到室温.
②
调节量筒使其液面与E装置中的液面持平
调节量筒使其液面与E装置中的液面持平
,③
读曲量筒中液体体积时,视线与液体的凹液面相平
读曲量筒中液体体积时,视线与液体的凹液面相平
.(4)通过计算,推断出该条件下反应的化学方程式
3CuSO4
3CuO+2SO2↑+SO3↑+O2↑
| ||
3CuSO4
3CuO+2SO2↑+SO3↑+O2↑
.
| ||
分析:I.(1)由题意可知,铜粉投入盛有稀硫酸的容器,缓缓鼓入氧气,溶液慢慢变蓝色,说明生成硫酸铜,根据元素守恒可知还生成水;
在溶液中放置些铂丝,形成原电池,反应速率加快;
从溶液中获得晶体,需要加热蒸发、冷却结晶、洗涤、干燥等;
(2)铜不能与硫酸亚铁反应,方案错误;Cu和氧气反应需要加热,消耗能量,无污染;铜和浓硫酸反应生成二氧化硫,由污染;根据可持续发展的原则判断最佳方案;
II.(1)加热硫酸铜生成三氧化硫和氧气、二氧化硫、和氧化铜,硫酸能和亚硫酸氢钠反应生成二氧化硫;
(2)浓硫酸具有吸水性,能干燥酸性或中性气体;
(3)根据水面的特点明确量筒中液体体积的读数方法;
(4)通过计算确定生成物之间的物质的量关系,再根据原子守恒确定反应方程式.
在溶液中放置些铂丝,形成原电池,反应速率加快;
从溶液中获得晶体,需要加热蒸发、冷却结晶、洗涤、干燥等;
(2)铜不能与硫酸亚铁反应,方案错误;Cu和氧气反应需要加热,消耗能量,无污染;铜和浓硫酸反应生成二氧化硫,由污染;根据可持续发展的原则判断最佳方案;
II.(1)加热硫酸铜生成三氧化硫和氧气、二氧化硫、和氧化铜,硫酸能和亚硫酸氢钠反应生成二氧化硫;
(2)浓硫酸具有吸水性,能干燥酸性或中性气体;
(3)根据水面的特点明确量筒中液体体积的读数方法;
(4)通过计算确定生成物之间的物质的量关系,再根据原子守恒确定反应方程式.
解答:解:I.(1)将铜粉投入盛有稀硫酸的容器中,无反应.向容器底部缓缓鼓入氧气,溶液慢慢变蓝色,说明溶液中含有硫酸铜,即铜和氧气、硫酸反应生成硫酸铜和水,反应方程式为2Cu+O2+2H2SO4=2CuSO4+2H2O;
铜、铂丝和氧气、稀硫酸构成原电池,加快了化学反应速率,负极上铜失电子,正极上氧气得电子和氢离子反应生成水;
从溶液中制取晶体的方法是采用蒸发、冷却结晶、过滤、洗涤的方法,
故答案为:2Cu+O2+2H2SO4=2CuSO4+2H2O;形成了原电池;加热蒸发、冷却结晶、过滤并洗涤晶体;
(2)乙中Cu和氧气反应需要加热,消耗能量;
丙中铜不能与硫酸亚铁反应,方案错误;
丁中铜和硝酸银反应制取硝酸铜,硝酸银的价格较高,所以耗资大;
戊中铜和浓硫酸反应需要 加热消耗能量高,且反应过程中生成的二氧化硫有毒,有污染;
根据可持续发展的原则可知最佳方案为甲,
故答案为:丙;戊;乙;甲;
Ⅱ、(1)加热硫酸铜生成氧化铜、三氧化硫、二氧化硫和氧气,三氧化硫易溶于水生成硫酸,硫酸能和亚硫酸氢钠反应生成二氧化硫,所以亚硫酸氢钠的作用是吸收SO3,放出等物质的量的SO2,
故答案为:吸收SO3,放出等物质的量的SO2;
(2)气体通过D装置后还剩二氧化硫和氧气、水蒸气,水蒸气能影响实验的测定,所以必须通过干燥剂吸收水分,所以浓硫酸的作用是:吸收水分,干燥SO2和O2,
故答案为:吸收水分,干燥SO2和O2;
(3)测定气体体积时,应装置内气体的温度应恢复到室温,调节量筒使其液面与E装置中的液面持平,由于量筒中液面是凹液面,所以读量筒中液体体积时,视线与液体的凹液面相平,否则会造成误差,
故答案为:②调节量筒使其液面与E装置中的液面持平;③读曲量筒中液体体积时,视线与液体的凹液面相平;
(4)干燥管C吸收的物质是二氧化硫,二氧化硫包括解热硫酸铜生成的二氧化硫和三氧化硫和水、亚硫酸氢钠反应生成的二氧化硫,二氧化硫的物质的量是
=0.0375mol,根据三氧化硫和亚硫酸氢钠之间的关系式知,三氧化硫和亚硫酸氢钠反应生成的二氧化硫和三氧化硫的物质的量相等,所以三氧化硫和原生成的二氧化硫的物质的量之和是0.0375mol;测得量筒B中水的体积,得出气体在标准状况下的体积为280mL,该气体是氧气,其物质的量是
=0.0125mol,根据氧化还原反应中得失电子数相等知,原生成的二氧化硫的物质的量=
=0.025mol,所以生成的三氧化硫的物质的量是0.0375mol-0.025mol=0.0125mol;6g无水CuSO4的物质的量=
=0.0375mol,根据铜原子守恒知,生成氧化铜的物质的量是0.0375mol,所以n(CuSO4):n(CuO):n(SO2):n(SO3):n(O2)=0.0375mol:0.0375mol:0.025mol:0.0125mol:0.0125mol=3:3:2:1:1,所以其分解方程式为3CuSO4
3CuO+2SO2↑+SO3↑+O2↑,
故答案为:3CuSO4
3CuO+2SO2↑+SO3↑+O2↑.
铜、铂丝和氧气、稀硫酸构成原电池,加快了化学反应速率,负极上铜失电子,正极上氧气得电子和氢离子反应生成水;
从溶液中制取晶体的方法是采用蒸发、冷却结晶、过滤、洗涤的方法,
故答案为:2Cu+O2+2H2SO4=2CuSO4+2H2O;形成了原电池;加热蒸发、冷却结晶、过滤并洗涤晶体;
(2)乙中Cu和氧气反应需要加热,消耗能量;
丙中铜不能与硫酸亚铁反应,方案错误;
丁中铜和硝酸银反应制取硝酸铜,硝酸银的价格较高,所以耗资大;
戊中铜和浓硫酸反应需要 加热消耗能量高,且反应过程中生成的二氧化硫有毒,有污染;
根据可持续发展的原则可知最佳方案为甲,
故答案为:丙;戊;乙;甲;
Ⅱ、(1)加热硫酸铜生成氧化铜、三氧化硫、二氧化硫和氧气,三氧化硫易溶于水生成硫酸,硫酸能和亚硫酸氢钠反应生成二氧化硫,所以亚硫酸氢钠的作用是吸收SO3,放出等物质的量的SO2,
故答案为:吸收SO3,放出等物质的量的SO2;
(2)气体通过D装置后还剩二氧化硫和氧气、水蒸气,水蒸气能影响实验的测定,所以必须通过干燥剂吸收水分,所以浓硫酸的作用是:吸收水分,干燥SO2和O2,
故答案为:吸收水分,干燥SO2和O2;
(3)测定气体体积时,应装置内气体的温度应恢复到室温,调节量筒使其液面与E装置中的液面持平,由于量筒中液面是凹液面,所以读量筒中液体体积时,视线与液体的凹液面相平,否则会造成误差,
故答案为:②调节量筒使其液面与E装置中的液面持平;③读曲量筒中液体体积时,视线与液体的凹液面相平;
(4)干燥管C吸收的物质是二氧化硫,二氧化硫包括解热硫酸铜生成的二氧化硫和三氧化硫和水、亚硫酸氢钠反应生成的二氧化硫,二氧化硫的物质的量是
| 2.4g |
| 64g/mol |
| 0.28l |
| 22.4L/mol |
| 0.0125mol×4 |
| 2 |
| 6g |
| 160g/mol |
| ||
故答案为:3CuSO4
| ||
点评:本实验题综合性较强,考查了电化学知识、硫酸铜的制备、环境知识、实验基本操作等,难度较大,难点是确定硫酸铜的分解方程式的书写,注意碱石灰吸收的二氧化硫有部分是硫酸铜分解生成的、部分是三氧化硫和水、亚硫酸氢钠反应生成的二氧化硫,否则会导致计算错误.

练习册系列答案
相关题目