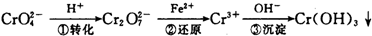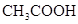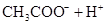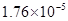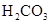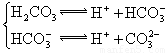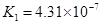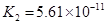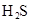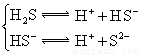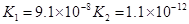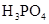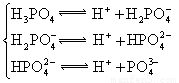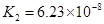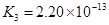题目内容
计算下列溶液的pH值:(lg2=0.3,lg5=0.7溶液的体积变化忽略不计)
(1)若pH为2和pH为6两盐酸等体积混合,则混合后PH=
(2)若pH为9和pH为13两NaOH溶液等体积混合,则混合后PH=
(3)若pH为13的强碱溶液和pH为2的强酸溶液以1:9体积比混合,则混合后pH=
(1)若pH为2和pH为6两盐酸等体积混合,则混合后PH=
2.3
2.3
;(2)若pH为9和pH为13两NaOH溶液等体积混合,则混合后PH=
12.7
12.7
;(3)若pH为13的强碱溶液和pH为2的强酸溶液以1:9体积比混合,则混合后pH=
11
11
.分析:(1)pH为2和pH为6的盐酸中c(H+)分别为:0.01mol/L、10-6 mol/L,先计算混合溶液中c(H+),再根据pH计算方法计算混合溶液的pH;
(2)pH=9的氢氧化钠溶液中c(OH-)=10-5 mol/L,pH=13的氢氧化钠溶液中c(OH-)=0.1mol/L,先计算混合溶液中c(OH-),再根据c(H+)=
,从而得出溶液的pH;
(3)pH=13的强碱溶液中c(OH-)=0.1mol/L,pH=2的强酸溶液c(H+)=0.01mol/L,二者以1:9体积比混合,n(碱)>n(酸),所以强碱有剩余,混合溶液中c(OH-),再根据c(H+)=
,从而得出溶液的pH.
(2)pH=9的氢氧化钠溶液中c(OH-)=10-5 mol/L,pH=13的氢氧化钠溶液中c(OH-)=0.1mol/L,先计算混合溶液中c(OH-),再根据c(H+)=
| KW |
| c(OH-) |
(3)pH=13的强碱溶液中c(OH-)=0.1mol/L,pH=2的强酸溶液c(H+)=0.01mol/L,二者以1:9体积比混合,n(碱)>n(酸),所以强碱有剩余,混合溶液中c(OH-),再根据c(H+)=
| KW |
| c(OH-) |
解答:解:(1)pH为2和pH为6的盐酸中c(H+)分别为:0.01mol/L、10-6 mol/L,二者等体积混合,混合溶液中c(H+)=
mol/L,pH=-lg
=2.3,
故答案为:2.3;
(2)pH=9的氢氧化钠溶液中c(OH-)=10-5 mol/L,pH=13的氢氧化钠溶液中c(OH-)=0.1mol/L,二者等体积混合,混合溶液中c(OH-)=
mol/L,c(H+)=
=
mol/L,pH=-lg
=12.7,
故答案为:12.7;
(3)pH=13的强碱溶液中c(OH-)=0.1mol/L,pH=2的强酸溶液c(H+)=0.01mol/L,二者以1:9体积比混合,n(碱)>n(酸),所以强碱有剩余,混合溶液中c(OH-)=
mol/L=0.001mol/L,c(H+)=
=
mol/L=10-11 mol/L,所以pH=-lg10-11=11,
故答案为:11.
| 10-2+10-6 |
| 2 |
| 10-2+10-6 |
| 2 |
故答案为:2.3;
(2)pH=9的氢氧化钠溶液中c(OH-)=10-5 mol/L,pH=13的氢氧化钠溶液中c(OH-)=0.1mol/L,二者等体积混合,混合溶液中c(OH-)=
| 10-5+0.1 |
| 2 |
| KW |
| c(OH-) |
| 10-14 | ||
|
| 2×10-14 |
| 10-5+0.1 |
故答案为:12.7;
(3)pH=13的强碱溶液中c(OH-)=0.1mol/L,pH=2的强酸溶液c(H+)=0.01mol/L,二者以1:9体积比混合,n(碱)>n(酸),所以强碱有剩余,混合溶液中c(OH-)=
| 0.1×1-0.01×9 |
| 10 |
| KW |
| c(OH-) |
| 10-14 |
| 0.001 |
故答案为:11.
点评:本题考查了酸、碱溶液中pH的简单计算,先计算混合溶液中氢离子浓度,再根据pH公式计算溶液pH,难度不大.

练习册系列答案
相关题目
对于弱酸,在一定温度下达到电离平衡时,各微粒的浓度存在一种定量的关系.下表是25℃时几种常见弱酸的电离平衡常数
|
酸 |
电离方程式 |
电离平衡常数K |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
回答下列各问:
(1)K只与温度有关,当温度升高时,K值________(填“增大”、“减小”、“不变”).
(2)在温度相同时,各弱酸的K值不同,那么K值的大小与酸性的相对强弱有何关系?__________________.
(3)若把CH3COOH、H2CO3、HCO3-、H2S、HS-、H3PO4、H2PO4-、HPO42-都看作是酸,其中酸性最强的是_________,最弱的是________.
(4)多元弱酸是分步电离的,每一步都有相应的电离平衡常数.对于同一种多元弱酸的K1、K2、K3之间存在着数量上的规律,对于H3PO4此规律是________________,产生此规律的原因是_________________________.
 (5)电离平衡常数是用实验的方法测定出来的.现已经测得某温度下 NH3∙H2O溶液中存在如下反应:NH3∙H2O NH4++OH-
已知0.10 mol·L-1
NH3∙H2O溶液中,达到平衡时,C平衡(OH-)=4.2 × 10-3mol·L-1,C平衡(NH3∙H2O)≈C起始(NH3∙H2O),水的电离可忽略不计;
(5)电离平衡常数是用实验的方法测定出来的.现已经测得某温度下 NH3∙H2O溶液中存在如下反应:NH3∙H2O NH4++OH-
已知0.10 mol·L-1
NH3∙H2O溶液中,达到平衡时,C平衡(OH-)=4.2 × 10-3mol·L-1,C平衡(NH3∙H2O)≈C起始(NH3∙H2O),水的电离可忽略不计;
①用pH试纸测量溶液的pH值,即可求得C平衡(OH-),测定溶液pH值的操作是______________。
②测量C平衡(NH3∙H2O)的方法最好用_____________法(填方法名称)
③求此温度下该反应的平衡常数K.(写出计算过程,计算结果保留2位有效数字)
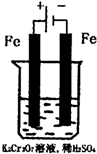 环境中常见的重金属污染有:汞、铅、锰、铬、镉.处理工业废水中常含有的Cr2O72-和CrO
环境中常见的重金属污染有:汞、铅、锰、铬、镉.处理工业废水中常含有的Cr2O72-和CrO