题目内容
19.标准状况下,V L的某气体(摩尔质量为M g•mol-1)溶解在1L水(水的密度近似为1g•cm-3)中,假设气体完全溶解且不与水发生反应,溶液的密度为ρg•cm-3,则所得溶液的物质的量浓度c=$\frac{1000ρV}{22400+VM}$mol/L.(选择以上字母表达计算式,要求化简).分析 根据n=$\frac{V}{{V}_{m}}$计算气体物质的量,根据m=nM计算气体质量,溶液质量=气体质量+水的质量,根据V=$\frac{m}{ρ}$计算溶液体积,再根据c=$\frac{n}{V}$计算溶液物质的量浓度.
解答 解:标准状况下,V L的某气体的物质的量为$\frac{VL}{22.4L/mol}$=$\frac{V}{22.4}$mol,
气体质量为$\frac{V}{22.4}$mol×M g•mol-1=$\frac{VM}{22.4}$g,
溶液质量为:1000mL×1g•cm-3+$\frac{VM}{22.4}$g=(1000+$\frac{VM}{22.4}$)g,
溶液体积为$\frac{(1000+\frac{VM}{22.4})g}{1000ρg/L}$=$\frac{22400+VM}{22400ρ}$L,
故溶液的物质的量浓度为$\frac{\frac{V}{22.4}}{\frac{22400+VM}{22400ρ}L}$=$\frac{1000ρV}{22400+VM}$mol/L,
故答案为:$\frac{1000ρV}{22400+VM}$.
点评 本题考查物质的量浓度计算,注意对定义式的理解,关键是计算溶液的体积.

练习册系列答案
相关题目
9.有关合金的性质叙述不正确的是( )
| A. | 合金的熔点比它的各成分的熔点低 | B. | 合金一定是金属熔合而成 | ||
| C. | 合金的硬度和强度一般比纯金属高 | D. | 硬铝、黄铜、钢均为合金 |
4.在无色溶液中能大量共存的一组离子是( )
| A. | Ag+、Cl-、NO3-、K+ | B. | K+、Cu2+、SO42-、NO3- | ||
| C. | K+、Mg2+、Cl-、OH- | D. | NH4+、SO42-、NO3-、Na+ |
8.常温下能与水反应的金属单质是( )
| A. | SiO2 | B. | Br2 | C. | Na2O | D. | Na |


 $\stackrel{-H_{2}O}{→}$
$\stackrel{-H_{2}O}{→}$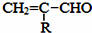
 的相对分子质量大2,则符合下列条件的G的同分异构体有3种.
的相对分子质量大2,则符合下列条件的G的同分异构体有3种. 的合成路线
的合成路线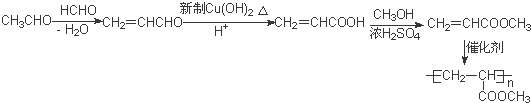 .
.