题目内容
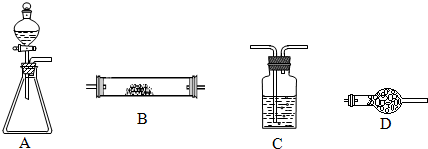
如图所示是用于气体制备、干燥、性质验证、尾气处理的部分仪器装置(加热及夹持固定装置均已略去).请根据下列要求回答问题.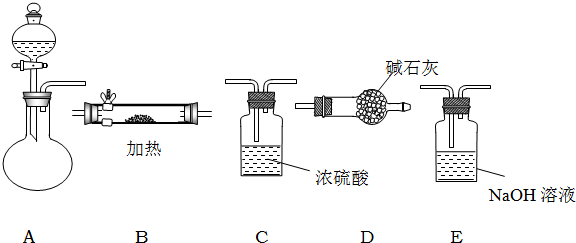
(1)若烧瓶中盛装锌片,分液漏斗中盛装稀硫酸,则:
①当仪器连接顺序为A→C→B→B→D时,两次使用B装置,其中所盛的药品依次是CuO、无水CuSO4粉末.其作用分别是
②D装置的作用是
③加热前必须进行的操作是
(2)若烧瓶中盛装Na2O2固体,分液漏斗中盛装浓氨水,慢慢打开分液漏斗的活塞,则:
①烧瓶内产生的气体主要有(写化学式)
②用产生的气体经干燥后做氨的催化氧化实验,B内放置铂铑合金网,各仪器装置按气流方向从左到右连接顺序是(填字母)(
分析:(1)①装置A中产生的氢气被浓硫酸干燥后通过灼热的氧化铜,由于氢气具有还原性能将氧化铜还原为铜,通过无水硫酸铜验证水的生成,最后连接装置D是为了防止空气中的水蒸气进入盛有无水硫酸铜的装置B中,可见此实验的目的是验证氢气的还原性和检验氧化产物;
②连接装置D是为了防止空气中的水蒸气进入盛有无水硫酸铜的装置B中;
③由于氢气与空气的混合气体点燃易爆炸,所以点燃前需要对气体进行验纯;
(2)①过氧化钠与水反应生成氧气;依据一水合氨存在电离平衡,改变条件平衡发生移动;
②NH3被O2氧化生成NO,剩余气体必须进行尾气处理,D盛装碱石灰,吸收氨气,NH3被O2氧化则证明氨气具有还原性;
②连接装置D是为了防止空气中的水蒸气进入盛有无水硫酸铜的装置B中;
③由于氢气与空气的混合气体点燃易爆炸,所以点燃前需要对气体进行验纯;
(2)①过氧化钠与水反应生成氧气;依据一水合氨存在电离平衡,改变条件平衡发生移动;
②NH3被O2氧化生成NO,剩余气体必须进行尾气处理,D盛装碱石灰,吸收氨气,NH3被O2氧化则证明氨气具有还原性;
解答:解:(1)①当仪器连接顺序为A→C→B→B→D时,两次使用B装置,其中所盛的药品依次是CuO、无水CuSO4粉末,装置A中产生的氢气被浓硫酸干燥后通过灼热的氧化铜,由于氢气具有还原性能将氧化铜还原为铜,通过无水硫酸铜验证水的生成,最后连接装置D是为了防止空气中的水蒸气进入盛有无水硫酸铜的装置B中,可见此实验的目的是验证氢气的还原性和检验氧化产物,
故答案为:验证氢气的还原性并检验其氧化产物水;
②D装置装有碱石灰,碱石灰的成分为氧化钙和氢氧化钠,能吸收水和二氧化碳,该实验的目的为验证氢气的还原性并检验其氧化产物水,防止空气中的水进入装置,干扰水的检验,需用装置D,
故答案为:防止空气中的水进入装置,干扰水的检验;
③由于氢气与空气的混合气体点燃易爆炸,所以点燃前需要对气体进行验纯,
故答案为:检验装置中空气是否排尽或检验氢气是否纯净;
(2)①过氧化钠与水反应2Na2O2 +2H2O═4NaOH+O2↑,放热,在氨水中存在平衡NH3+H2O?NH3?H2O?NH4++OH-,加入氢氧化钠,氢氧根离子浓度增大,平衡左移有利于氨气放出,放热也有利于氨气放出,
故答案为:O2、NH3;
②过氧化钠与水反应生成氧气,与氨气经盛有碱石灰的干燥管干燥后在催化剂的作用下反应4NH3+5O2
4NO+6H2O,生成NO,剩余气体必须进行尾气处理,则连接顺序为A→D→B→D(D盛装碱石灰),NO和氧气反应生成红棕色的二氧化氮气体,在B中可观察到红棕色,NH3被O2氧化则证明氨气具有还原性,
故答案为:A→D→B→D;有大量红棕色气体出现;还原;
故答案为:验证氢气的还原性并检验其氧化产物水;
②D装置装有碱石灰,碱石灰的成分为氧化钙和氢氧化钠,能吸收水和二氧化碳,该实验的目的为验证氢气的还原性并检验其氧化产物水,防止空气中的水进入装置,干扰水的检验,需用装置D,
故答案为:防止空气中的水进入装置,干扰水的检验;
③由于氢气与空气的混合气体点燃易爆炸,所以点燃前需要对气体进行验纯,
故答案为:检验装置中空气是否排尽或检验氢气是否纯净;
(2)①过氧化钠与水反应2Na2O2 +2H2O═4NaOH+O2↑,放热,在氨水中存在平衡NH3+H2O?NH3?H2O?NH4++OH-,加入氢氧化钠,氢氧根离子浓度增大,平衡左移有利于氨气放出,放热也有利于氨气放出,
故答案为:O2、NH3;
②过氧化钠与水反应生成氧气,与氨气经盛有碱石灰的干燥管干燥后在催化剂的作用下反应4NH3+5O2
| ||
| 加热 |
故答案为:A→D→B→D;有大量红棕色气体出现;还原;
点评:本题以氨气的催化氧化为载体考查物质制备实验,掌握反应原理,理清装置连接,把握实验气体制备、含有杂质的验证和除杂方法和步骤是解题关键,题目难度中等.

练习册系列答案
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案 新思维寒假作业系列答案
新思维寒假作业系列答案
相关题目
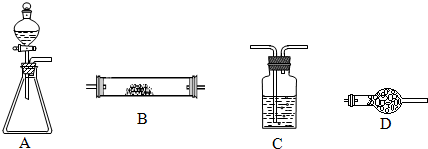
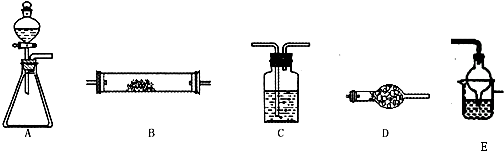
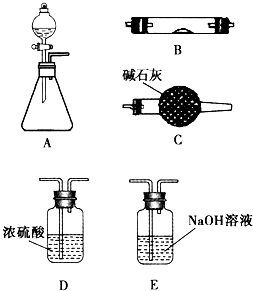 如图所示是用于气体制备、干燥、性质验证、尾气处理的部分仪器装置(加热及夹持装置均已略去).请根据下列要求回答问题.
如图所示是用于气体制备、干燥、性质验证、尾气处理的部分仪器装置(加热及夹持装置均已略去).请根据下列要求回答问题.