题目内容
20.下列物质中所含分子数最多的是( )| A. | 56 g N2 | B. | 3.01×1023个硫酸分子 | ||
| C. | 标准状况下 22.4 LCl2 | D. | 1.5 molO2 |
分析 先根据n=$\frac{m}{M}$=$\frac{N}{{N}_{A}}$=$\frac{V}{{V}_{m}}$将选项中的各量转化成物质的量,根据N=nNA可知物质的量越大,含有的分子数越多,据此进行解答.
解答 解:A.56gN2的物质的量为:$\frac{56g}{28g/mol}$=2mol;
B.3.01×1023个硫酸分子的物质的量为:$\frac{3.01×1{0}^{23}}{6.02×1{0}^{23}mo{l}^{-1}}$=0.5mol;
C.标准状况下22.4LCl2的物质的量为:$\frac{22.4L}{22.4L/mol}$=1mol;
D.1.5 molO2;
根据N=nNA可知物质的量越大,含有的分子数越多,则含有分子数最多的为A,
故选A.
点评 本题考查物质的量的计算,题目难度不大,明确物质的量与其它物理量之间的关系为解答关键,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
19.下列关于有机化合物的说法正确的是( )
| A. | C2H6和C3H8不存在同分异构体,CH2O和C2H4O2互为同系物 | |
| B. | 一定条件下,乙烯、乙酸乙酯和淀粉都能与水反应 | |
| C. | 乙烯和苯分子中都含有碳碳双键,都能使溴水褪色 | |
| D. | 糖类、油脂和蛋白质都能发生水解 |
8.工业上曾经通过反应“3Fe+4NaOH $\stackrel{1100℃}{?}$Fe3O4+2H2↑+4Na↑”生产金属钠,己知铁的熔点1535℃、沸点3000℃.下列有关说法正确的是( )
| A. | 每生成1mol H2,转移的电子数约为4NA | |
| B. | 增大铁的量可以使反应速率加快 | |
| C. | 该反应条件下铁的金属性比钠强 | |
| D. | 将生成的气体在空气中冷却可获得钠 |
15.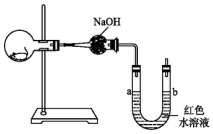 如图所示,烧瓶内有一只活的小白鼠,U形管内装有红色水溶液,使a、b两端的液面处于同一水平面.经数小时后,U形管a、b两处的液面会出现下列哪种情况(实验装置足以维持实验期间小白鼠的生命活动,瓶口密封,忽略水蒸气和温度变化对实验结果的影响)( )
如图所示,烧瓶内有一只活的小白鼠,U形管内装有红色水溶液,使a、b两端的液面处于同一水平面.经数小时后,U形管a、b两处的液面会出现下列哪种情况(实验装置足以维持实验期间小白鼠的生命活动,瓶口密封,忽略水蒸气和温度变化对实验结果的影响)( )
 如图所示,烧瓶内有一只活的小白鼠,U形管内装有红色水溶液,使a、b两端的液面处于同一水平面.经数小时后,U形管a、b两处的液面会出现下列哪种情况(实验装置足以维持实验期间小白鼠的生命活动,瓶口密封,忽略水蒸气和温度变化对实验结果的影响)( )
如图所示,烧瓶内有一只活的小白鼠,U形管内装有红色水溶液,使a、b两端的液面处于同一水平面.经数小时后,U形管a、b两处的液面会出现下列哪种情况(实验装置足以维持实验期间小白鼠的生命活动,瓶口密封,忽略水蒸气和温度变化对实验结果的影响)( )| A. | a端下降,b端上升 | B. | a端上升,b端下降 | C. | a、b两端都下降 | D. | a、b两端都上升 |
12.下列各溶液中,微粒的物质的量浓度关系正确的是( )
| A. | 向硝酸钠溶液中滴加稀盐酸得到的pH=5的混合溶液:c(Na+)=c(NO3-) | |
| B. | 0.1 mol/L NH4Cl溶液:c(NH4+ )=c(Cl-) | |
| C. | 向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) | |
| D. | 0.1mol AgCl和0.1molAgI混合后加入100mL水中,所得溶液中c(Cl-)=c(I-) |
9.下列说法中错误的是( )
| A. | 离子化合物中阴阳离子间存在静电引力和静电斥力 | |
| B. | 在NH4+和[Cu(NH3)4]2+中都存在配位键 | |
| C. | 元素电负性越大的原子,吸引电子的能力越强 | |
| D. | ClO3-的空间构型为平面三角形 |
 如图是一个化学过程的示意图.已知甲池的总反应式为:2CH3OH+3O2+4KOH$?_{充电}^{放电}$2K2CO3+6H2O
如图是一个化学过程的示意图.已知甲池的总反应式为:2CH3OH+3O2+4KOH$?_{充电}^{放电}$2K2CO3+6H2O