题目内容
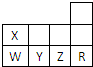 表为元素周期表前三周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )
表为元素周期表前三周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )| A、常压下五种元素的单质中Z单质的沸点最高 | B、Y、Z、W的阴离子的还原性强弱顺序为:Z->Y2->W3- | C、最高价含氧酸的酸性强弱顺序为:H2YO4>HZO4>H3WO4 | D、五种元素对应的单质固态时均为分子晶体 |
分析:元素周期表前三周期的一部分,根据元素在周期表中的位置知,X、Y、Z、W、R分别是N、S、Cl、P、Ar元素,
A.根据常温下单质存在的状态判断;
B.电子层结构相同的阴离子中,阴离子半径随着原子序数序数的增大而减小;
C.元素的非金属性越强,其最高价氧化物的水化物酸性越强,同一周期中,元素的非金属性随着原子序数的增大而增强;
D.根据晶体的构成微粒判断.
A.根据常温下单质存在的状态判断;
B.电子层结构相同的阴离子中,阴离子半径随着原子序数序数的增大而减小;
C.元素的非金属性越强,其最高价氧化物的水化物酸性越强,同一周期中,元素的非金属性随着原子序数的增大而增强;
D.根据晶体的构成微粒判断.
解答:解:A.元素周期表前三周期的一部分,根据元素在周期表中的位置知,X、Y、Z、W、R分别是N、S、Cl、P、Ar元素,
A.这几种元素形成的晶体都是分子晶体,常温下沸点最高的是硫单质,所以Y单质的沸点最高,故A错误;
B.电子层结构相同的阴离子中,阴离子半径随着原子序数序数的增大而减小,所以Y、Z、W的阴离子的还原性强弱顺序为:Z-<Y2-<W3-,故B错误;
C.元素的非金属性越强,其最高价氧化物的水化物酸性越强,同一周期中,元素的非金属性随着原子序数的增大而增强,所以这几种元素的非金属性强弱顺序是W<Y<Z,则最高价含氧酸的酸性强弱顺序为:HZO4>H2YO4>H3WO4,故C错误;
D.这几种元素的单质中,其晶体的构成微粒都是分子,所以都是分子晶体,故D正确;
故选D.
A.这几种元素形成的晶体都是分子晶体,常温下沸点最高的是硫单质,所以Y单质的沸点最高,故A错误;
B.电子层结构相同的阴离子中,阴离子半径随着原子序数序数的增大而减小,所以Y、Z、W的阴离子的还原性强弱顺序为:Z-<Y2-<W3-,故B错误;
C.元素的非金属性越强,其最高价氧化物的水化物酸性越强,同一周期中,元素的非金属性随着原子序数的增大而增强,所以这几种元素的非金属性强弱顺序是W<Y<Z,则最高价含氧酸的酸性强弱顺序为:HZO4>H2YO4>H3WO4,故C错误;
D.这几种元素的单质中,其晶体的构成微粒都是分子,所以都是分子晶体,故D正确;
故选D.
点评:本题考查了元素周期表和元素周期律的综合应用,根据元素在周期表中的位置确定元素,再结合结构和元素周期律来分析解答,知道简单离子半径的比较方法,难度不大.

练习册系列答案
相关题目