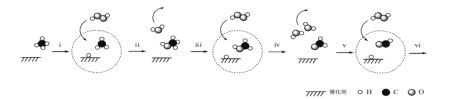
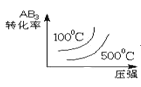
��Ŀ����
����Ŀ�����Ĺ̶��͵���ѭ���Ǽ���������ѧ��һֱ�о��Ŀ��⡣
(1)�±��о��˲�ͬ�¶��´����̵���ҵ�̵��IJ���K ֵ��
��Ӧ | �����̵�N2(g)+O2(g) | ��ҵ�̵�N2(g)+3H2(g) | |||
�¶�/�� | 27 | 2000 | 25 | 400 | 450 |
K | 3.84��10-31 | 0.1 | 5��108 | 0.507 | 0.152 |
�ٷ������ݿ�֪������ʺϴ��ģģ������̵���ԭ��____��
�ڴ�ƽ���ӽǿ��ǹ�ҵ�̵�Ӧ��ѡ������������ʵ�ʹ�ҵ����ȴѡ�� 500�����ҵĸ��£� ��������ܵ�ԭ��_____��
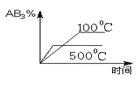
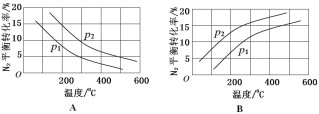
(2)��ҵ�̵���Ӧ�У�������������ͬʱ���ֱ�ⶨ N2 ��ƽ��ת�����ڲ�ͬѹǿ(��1����2)�����¶ȱ仯�����ߣ���ͼ��ʾ��ͼʾ�У���ȷ����_____(�A����B��)���Ƚ���1����2�Ĵ�С��ϵ_____��
(3)��ͼ��ijѹǿ�£�N2 ��H2 �������1��3Ͷ��ʱ����Ӧ������а�������������¶ȵı仯���ߡ�����һ���Ǿ���һ��ʱ�䷴Ӧ������ߣ���һ����ƽ��ʱ�����ߡ�
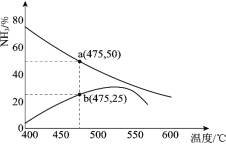
��ͼ��b �㣬v(��)_____v(��)��(�����������������)
��ͼ��a �㣬���������� n(N2):n(NH3)=_____��
(4)��֪��N2(g)+3H2(g)![]() 2NH3(g)��H����92.4kJ��mol��1��2H2(g) +O2(g)
2NH3(g)��H����92.4kJ��mol��1��2H2(g) +O2(g)![]() 2H2O(l)��H����575.6kJ��mol��1�����꣬���п�ѧ������ڳ��¡���ѹ�������������µ�����Һ̬ˮ�ϳɰ�����ͬʱ������������˼·����÷�Ӧ���Ȼ�ѧ��Ӧ����ʽΪ��_____��
2H2O(l)��H����575.6kJ��mol��1�����꣬���п�ѧ������ڳ��¡���ѹ�������������µ�����Һ̬ˮ�ϳɰ�����ͬʱ������������˼·����÷�Ӧ���Ȼ�ѧ��Ӧ����ʽΪ��_____��
(5)NH3��һ�������¿ɱ�������
��֪������4NH3(g)+3O2(g)��2N2(g)+6H2O(g)��H����1298kJ/mol
����
�� �Ͽ� 1 mol H-O ����Ͽ� 1 mol H-N �������������Լ_____kJ��
�� H-O ���� H-N ��(�ǿ��������)_____��
���𰸡������̵�Ϊ���ȷ�Ӧ���¶ȸߴ�2000��ʱ��Kֵ��Ȼ��С��������еij̶Ⱥ�С��ת���ʺܵͣ����ʺϴ��ģ���� �¶���500������ʱ����������ߣ���Ӧ���ʽϿ죬�ﵽƽ����Ҫ��ʱ��϶̣��ӷ�Ӧ���ʺʹ����Ļ��ԵȽǶȿ��ǣ�ѡ��500�����Ҹ����� A p2��p1 �� 1��4 2N2(g)+6H2O(l)4NH3(g)+3O2(g) ��H=+1542 kJmol-1 75 ǿ
��������
(1)�����¶ȶԻ�ѧƽ�ⳣ��K��Ӱ����K�ĺ���������
(2)�ϳɰ���ӦΪ���������С�ķ��ȷ�Ӧ������¶Ⱥ�ѹǿ��ƽ���ƶ���Ӱ��������
(3)����ͼ����Ӱ��ƽ������أ�a������������ƽ�����ߡ�b�����������Ǿ���һ��ʱ�䷴Ӧ������ߣ��������ʽ������
(4)���ݸ�˹���ɷ������
(5)�����ʱ���H=��Ӧ��ļ���֮��-������ļ���֮�ͼ�����
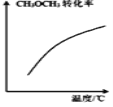
(1)���ɱ������ݿ�֪���ɱ������ݿ�֪���¶�Խ�ߣ������̵���Ӧ��KԽ��˵�������̵��ķ�ӦΪ���ȷ�Ӧ��2000��ʱ��K=0.1��Kֵ��С����ת���ʺ�С�����ʺϴ��ģ��������������ʺϴ��ģģ������̵����ʴ�Ϊ�������̵�Ϊ���ȷ�Ӧ���¶ȸߴ�2000��ʱ��Kֵ����С��������еij̶Ⱥ�С��ת���ʺܵͣ����ʺϴ��ģ������
���ɱ������ݿ�֪���¶�Խ�ߣ��ϳɰ���Ӧ��KԽС��˵���ϳɰ����ķ�ӦΪ���ȷ�Ӧ���ϳɰ���Ӧ�У��¶�Խ�ߣ���Ӧ����Խ�죬���Ǹ÷�ӦΪ���ȷ�Ӧ���¶ȸ�ת���ʻή�ͣ���500�����Ҵ���������ߣ����ԴӴ������Ե��ۺ����ؿ���ѡ��500����������ʣ��ʴ�Ϊ���¶���500�����Ҵ���������ߣ���Ӧ���ʽϿ죬�ﵽƽ����Ҫ��ʱ��϶̣��ӷ�Ӧ���ʺʹ����Ļ��ԵȽǶȿ��ǣ�ѡ��500�����Ҹ����ʣ�
(2)�ϳɰ���ӦΪ���ȷ�Ӧ�������¶ȣ�ƽ�������ƶ�����Ӧ���ת���ʼ�С������ͼA��ȷ��B����ӦN2 (g)+3H2 (g) 2NH3(g)��������Ϊ�����С�ķ�Ӧ������ѹǿ��ƽ�������ƶ���ת��������p2��ת���ʴ���p2�ʴ�Ϊ��A��p2��p1��
(3) ����ͼ֪��a������������ƽ�����ߡ�b�����������Ǿ���һ��ʱ�䷴Ӧ������ߡ�
��ͼ��b�㣬������������������ӣ���֪������Ӧ�����ƶ�������Ӧ���ʴ����淴Ӧ���ʣ��ʴ�Ϊ������
��ͼ��a�㣬�跴Ӧ��N2Ϊx��

ƽ��ʱ���������������Ϊ50%ʱ����![]() =50%����ã�x=
=50%����ã�x=![]() ����n(N2)��n(NH3)=
����n(N2)��n(NH3)=![]() ��
��![]() =1��4���ʴ�Ϊ��1��4��
=1��4���ʴ�Ϊ��1��4��
(4)��N2(g)+3H2(g)2NH3(g) ��H=-92.4kJmol-1����2H2(g)+O2(g)2H2O(l) ��H=-575.6kJmol-1���ɸ�˹���ɣ��١�2-�ڡ�3��2N2(g)+6H2O(l)4NH3(g)+3O2(g) ��H=(-92.4kJmol-1)��2-(-575.6kJmol-1)��3=+1542 kJmol-1���ʴ�Ϊ��2N2(g)+6H2O(l)4NH3(g)+3O2(g) ��H=+1542 kJmol-1��
(5)�ٸ���4NH3(g)+3O2(g)=2N2(g)+6H2O(g) ��H=-1298kJ/mol����֪12E(H-N)+3��498kJ/mol-2��946kJ/mol-12E(H-O)=-1298kJ/mol����E(H-O)- E(H-N)=75kJ/mol���ʴ�Ϊ��75��
�ڸ���E(H-O)- E(H-N)=75kJ/mol����֪H-O ����H-N��ǿ���ʴ�Ϊ��ǿ��

����Ŀ��ijʵ��С���FeCl3�ֱ���Na2SO3��NaHSO3�ķ�Ӧ����̽����
����ͬѧ��ʵ�飩
װ�� | ��� | �Լ�X | ʵ������ |
| I | Na2SO3��Һ(pH��9) | �պϿ��غ�����������ָ�뷢��ƫת |
II | NaHSO3��Һ(pH��5) | �պϿ��غ�����������ָ��δ����ƫת |
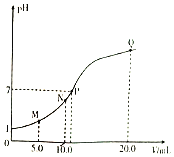
(1)����FeCl3��Һʱ���Ƚ�FeCl3����Ũ���ᣬ��ϡ����ָ��Ũ�ȡ���ϻ�ѧ����˵��Ũ��������ã���
(2)��ͬѧ̽��ʵ��I�ĵ缫����______________��
��ȡ����Na2SO3��Һ�缫�����Ļ��Һ������______________��������ɫ������֤��������![]() ��
��
�ڸ�ͬѧ�����ʵ��̽����һ�缫�IJ����ʵ�鷽��Ϊ______________��
(3)ʵ��I�и����ĵ缫��ӦʽΪ______________��
����ͬѧ��ʵ�飩
��ͬѧ��һ��̽��FeCl3��Һ��NaHSO3��Һ�ܷ�����Ӧ����ơ����ʵ�鲢��¼���£�
װ�� | ��� | ��Ӧʱ�� | ʵ������ |
| III | 0~1 min | ������ɫ�������д̼�����ζ�����ݳ� |
1~30 min | ����Ѹ���ܽ��γɺ�ɫ��Һ�������Һ��Ϊ��ɫ��֮����ɫ | ||
30 min�� | ������Ӵ����ֵ��ϲ���Һ�ֱ�Ϊdz��ɫ�������Ϊdz��ɫ |
(4)��ͬѧ��Ϊ�̼�����ζ����IJ���ԭ�������ֿ��ܣ������ӷ���ʽ��ʾ�ڵĿ���ԭ��
�� Fe3+��3![]()
![]() Fe(OH)3 ��3SO2����______________��
Fe(OH)3 ��3SO2����______________��
(5)�������ϣ���Һ��Fe3+��![]() ��OH�����������γɺ�ɫ����ﲢ��������ת����
��OH�����������γɺ�ɫ����ﲢ��������ת����
![]()
�ӷ�Ӧ���ʺͻ�ѧƽ�������ǶȽ���1~30 min��ʵ������______________��
(6)����30 min���ϲ���Һ�ֱ�Ϊdz��ɫ�Ŀ���ԭ��______________��
��ʵ�鷴˼��
(7)�ֱ�Ա�I��II��II��III��FeCl3�ܷ���Na2SO3��NaHSO3����������ԭ��Ӧ���й�(д������)______________��