题目内容
现有六种短周期元素A、B、C、D、E、F,其原子序数依次增大.A、E同主族,A元素原于半径是周期表中所有元素中最小的,B元素原子的最外层电子数是内层电子数的2倍.C元素最高价氧化物的水化物X能与其氢化物Y反应生成盐,F是地壳中含量最多的金属元素.A、B、C、E四种元素都能与D元素形成原子个数比不相同的常见化合物.?(1)写出Y和D2在催化剂作用下反应的化学方程式______△4NO+6H2O
【答案】分析:A元素原于半径是周期表中所有元素中最小的,则A为H元素,B元素原子的最外层电子数是内层电子数的2倍,应为C元素,C元素最高价氧化物的水化物X能与其氢化物Y反应生成盐,应为N元素,X为HNO3,Y为NH3,F是地壳中含量最多的金属元素,应为Al,A、E同主族,则E为Na元素,A、B、C、E四种元素都能与D元素形成原子个数比不相同的常见化合物,结合原子序数关系可知D为O元素,结合对应单质、化合物的性质解答该题.
解答:解:A元素原于半径是周期表中所有元素中最小的,则A为H元素,B元素原子的最外层电子数是内层电子数的2倍,应为C元素,C元素最高价氧化物的水化物X能与其氢化物Y反应生成盐,应为N元素,X为HNO3,Y为NH3,F是地壳中含量最多的金属元素,应为Al,A、E同主族,则E为Na元素,A、B、C、E四种元素都能与D元素形成原子个数比不相同的常见化合物,结合原子序数关系可知D为O元素,
(1)Y为NH3,与O2在催化剂的条件下反应生成NO和H2O,反应的化学方程式为4NH3+5O2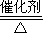 4NO+6H2O,
4NO+6H2O,
故答案为:4NH3+5O2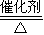 4NO+6H2O;
4NO+6H2O;
(2)将HNO3和NH3的水溶液充分混合后,常温下测得溶液的pH>7,说明溶液呈碱性,氨水过量,如氨水过量较小,则有c(NH4+)>c(NO3-)>c(OH-)>c(H+),如氨水过量较多,则存在c(NH4+)>c(OH-)>c(NO3-)>c(H+),
故答案为:c(NH4+)>c(NO3-)>c(OH-)>c(H+)或c(NH4+)>c(OH-)>c(NO3-)>c(H+);
(3)E为Na元素,对应的最高价氧化物的水化物为NaOH,F为Al,对应的氧化物为Al2O3,为两性氧化物,二者反应的离子方程式为Al2O3+2OH-=2AlO2-+H2O,
故答案为:Al2O3+2OH-=2AlO2-+H2O;
(4)用石墨电极电解NaOH溶液,实质上是电解的水,阳极反应为4OH-=2H2O+O2+4e-,
故答案为:4OH-=2H2O+O2+4e-;
(5)甲烷碱性燃料电池中,甲烷为原电池的负极,被氧化,电极反应式为CH4+10OH-=CO32-+6H2O+8e-,
n(CH4)=1mol时转移电子的物质的量为8mol,则可生成4molCl2,
故答案为:CH4+10OH-=CO32-+6H2O+8e-;4mol.
点评:本题考查原子结构与元素周期律的关系,题目难度中等,本题注意把握元素的种类的推断,为解答该题的关键,注意电极反应式的书写和相关计算,为易错点.
解答:解:A元素原于半径是周期表中所有元素中最小的,则A为H元素,B元素原子的最外层电子数是内层电子数的2倍,应为C元素,C元素最高价氧化物的水化物X能与其氢化物Y反应生成盐,应为N元素,X为HNO3,Y为NH3,F是地壳中含量最多的金属元素,应为Al,A、E同主族,则E为Na元素,A、B、C、E四种元素都能与D元素形成原子个数比不相同的常见化合物,结合原子序数关系可知D为O元素,
(1)Y为NH3,与O2在催化剂的条件下反应生成NO和H2O,反应的化学方程式为4NH3+5O2
 4NO+6H2O,
4NO+6H2O,故答案为:4NH3+5O2
 4NO+6H2O;
4NO+6H2O;(2)将HNO3和NH3的水溶液充分混合后,常温下测得溶液的pH>7,说明溶液呈碱性,氨水过量,如氨水过量较小,则有c(NH4+)>c(NO3-)>c(OH-)>c(H+),如氨水过量较多,则存在c(NH4+)>c(OH-)>c(NO3-)>c(H+),
故答案为:c(NH4+)>c(NO3-)>c(OH-)>c(H+)或c(NH4+)>c(OH-)>c(NO3-)>c(H+);
(3)E为Na元素,对应的最高价氧化物的水化物为NaOH,F为Al,对应的氧化物为Al2O3,为两性氧化物,二者反应的离子方程式为Al2O3+2OH-=2AlO2-+H2O,
故答案为:Al2O3+2OH-=2AlO2-+H2O;
(4)用石墨电极电解NaOH溶液,实质上是电解的水,阳极反应为4OH-=2H2O+O2+4e-,
故答案为:4OH-=2H2O+O2+4e-;
(5)甲烷碱性燃料电池中,甲烷为原电池的负极,被氧化,电极反应式为CH4+10OH-=CO32-+6H2O+8e-,
n(CH4)=1mol时转移电子的物质的量为8mol,则可生成4molCl2,
故答案为:CH4+10OH-=CO32-+6H2O+8e-;4mol.
点评:本题考查原子结构与元素周期律的关系,题目难度中等,本题注意把握元素的种类的推断,为解答该题的关键,注意电极反应式的书写和相关计算,为易错点.

练习册系列答案
相关题目