题目内容
18.X、Y、Z、W为四种短周期元素,已知X、Z同主族,Y、Z、W同周期;X的气态氢化物比Z的稳定;Y的阳离子比W的阳离子氧化性强;Y的阳离子比Z的阴离子少一个电子层.下列表示中,正确的是( )| A. | 原子序数:X>Y>Z>W | B. | 简单离子半径:W>Y>Z>X | ||
| C. | 原子半径:W>Y>Z>X | D. | 原子的得电子能力:X<Z |
分析 X、Y、Z、W为短周期元素,X、Z同主族,X的气态氢化物比Z的稳定,X、Z为非金属,非金属性:X>Z,原子序数Z>X,X处于第二周期,Z处于第三周期,Y、W同周期,Y的阳离子的氧化性小于W的阳离子的氧化性,二者为金属元素,金属性Y>W,原子序数Y<W,Y的阳离子比Z的阴离子少一个电子层,则Y、Z同周期,即Y、Z、W处于第三周期,结合元素周期律解答.
解答 解:X、Y、Z、W为短周期元素,X、Z同主族,X的气态氢化物比Z的稳定,X、Z为非金属,非金属性:X>Z,原子序数Z>X,X处于第二周期,Z处于第三周期,Y、W同周期,Y的阳离子的氧化性小于W的阳离子的氧化性,二者为金属元素,金属性Y>W,原子序数Y<W,Y的阳离子比Z的阴离子少一个电子层,则Y、Z同周期,即Y、Z、W处于第三周期.
A.由上述分析可知,原子序数Z>W>Y>X,故A错误;
B.电子层结构相同的离子,核电荷数越大离子半径越小,电子层越多离子半径越大,故离子半径Z>X>Y>W,故B错误;
C.同周期自左而右原子半径减小、同主族自上而下原子半径增大,故原子半径W>Y>Z>X,故C正确;
D.非金属性:X>Z,故得电子能力X<Z,故D错误,
故选:C.
点评 本题考查结构性质位置关系应用,侧重对元素周期律的考查,有利于基础知识的巩固.

练习册系列答案
 精英口算卡系列答案
精英口算卡系列答案
相关题目
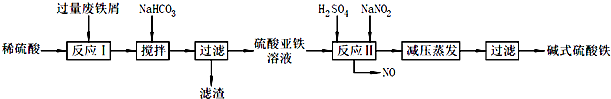
8.碱式硫酸铁[Fe(OH)SO4]是一种用于污水处理的新型高效絮凝剂,在医药上也可用于治疗消化性溃疡出血.工业上利用废铁屑(含少量氧化铝、氧化铁杂质)生产碱式硫酸铁的工艺流程如图:
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
下列说法不正确的是( )

已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
| A. | 加入少量NaHCO3的目的是调节pH,使溶液中的Al3+沉淀完全 | |
| B. | 该工艺中“搅拌”的作用是加快反应速率 | |
| C. | 在实际生产中,反应Ⅱ常同时通入O2以减少NaNO2的用量,若参与反应的O2有11.2L(标准状况),则相当于节约NaNO2的物质的量为2mol | |
| D. | 根据我国质量标准,产品中不得含有Fe2+,为了确定所得产品中是否含有Fe2+,所加试剂的顺序是先加KSCN溶液,后加氯水 |
9.C、N、S都是重要的非金属元素.下列说法正确的是( )
| A. | 三者对应的氧化物均为酸性氧化物 | |
| B. | 同浓度的Na2CO3、NaNO3、Na2SO3溶液的pH:NaNO3<Na2SO3<Na2CO3 | |
| C. | 三者的单质直接与氧气反应都能生成两种以上氧化物 | |
| D. | CO2、NO2、SO2都能与H2O反应,其反应原理相同 |
13.下列说法正确的是( )
| A. | 化合态的氟没有毒,含氟牙膏中的氟含量越多越好 | |
| B. | 火柴头中含有的氯元素为氯化钾 | |
| C. | 可用高锰酸钾来检测新装修居室内甲醛的浓度 | |
| D. | 火柴燃烧生成的气体不能使品红溶液褪色 |
3.下列各组大小顺序不正确的是( )
| A. | 粒子半径:Na+>Mg2+>S2->Cl- | B. | 热稳定性:SiH4<PH3<H2S<HCl | ||
| C. | 碱性强弱:KOH>NaOH>LiOH | D. | 还原性:HF<HCl<HBr<HI |
10.下列说法不正确的是( )
| A. | 当锌完全溶解后,铁与酸反应产生氢气的速率会显著减慢,此现象可作为判断镀锌铁皮中锌镀层是否完全被反应掉的依据 | |
| B. | “硝基苯制备”实验中,将温度计插入水浴,水银球不能与烧杯底部和烧杯壁接触 | |
| C. | 在酸碱中和滴定时,右手旋转滴定管的活塞,左手摇动锥形瓶,眼睛看滴定管的液面 | |
| D. | 除去干燥CO2中混有的少量SO2,可将混合气体依次通过盛有酸性KMnO4溶液、浓硫酸的洗气瓶 |
7.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 将1mol铁粉加入到一定量的稀硝酸溶液中充分反应,转移的电子数一定是3NA | |
| B. | 标准状况下,22.4L己烷中共价键数目为19NA | |
| C. | 由CO2和O2组成的混合物中共有NA个分子,其中的氧原子数为2NA | |
| D. | 1.0 L 1.0 mol•L-1 NaClO溶液中含有ClO-离子的数目为NA |
8.品红分子结构中的发色基团遇到SO2与水形成的亚硫酸后结构发生改变,生成不稳定的无色化合物.亚硫酸漂白原理可用下面的反应方程式表示下列说法不正确的是( )


| A. | 品红的分子式为C20H19N3 | |
| B. | 上述漂白原理反应属加成反应 | |
| C. | 碱性品红及其与H2SO3生成的无色化合物都可与NaOH溶液反应 | |
| D. | 碱性品红与H2SO3生成的无色化合物不稳定,加热后恢复原来的颜色 |