题目内容
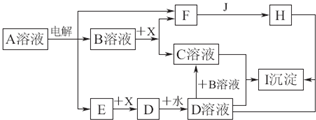
图中A~I分别表示化学反应中的一种常见物质,工业上常用电解A的饱和溶液的方法制取B.其中E、F、J在通常情况下是气体单质,E为有色气体,J是空气中含量最多的气体,X是一种常见的金属单质.部分产物和反应条件略去.
填写下列空白:
(1)写出电解A溶液的化学方程式:
(2)若将a mol D全部转化为C,则B的物质的量的取值范围为
(3)写出下列反应的离子方程式:
H+D→I:
B+X→C+F:
E与B溶液的反应:

填写下列空白:
(1)写出电解A溶液的化学方程式:
2NaCl+2H2O
Cl2↑+H2↑+2NaOH
| ||
2NaCl+2H2O
Cl2↑+H2↑+2NaOH
,电解过程中,向两极溶液中滴加酚酞试液,有一极溶液颜色变红,则该极为
| ||
阴
阴
(填“正”、“负”、“阴”或“阳”)极,该极的电极反应为2H++2e-═H2↑
2H++2e-═H2↑
.(2)若将a mol D全部转化为C,则B的物质的量的取值范围为
n(NaOH)≥4amol
n(NaOH)≥4amol
.(3)写出下列反应的离子方程式:
H+D→I:
3NH3?H2O+Al3+═Al(OH)3↓+3NH4+
3NH3?H2O+Al3+═Al(OH)3↓+3NH4+
;B+X→C+F:
2Al+2H2O+2OH-═2AlO2-+3H2↑
2Al+2H2O+2OH-═2AlO2-+3H2↑
;E与B溶液的反应:
Cl2+2OH-═Cl-+ClO-+H2O
Cl2+2OH-═Cl-+ClO-+H2O
.分析:E、F、J在通常情况下是气体单质,E为有色气体,E为Cl2.J是空气中含量最多的气体,则J为N2.工业上常用电解A的饱和溶液的方法制取B,电解过程中,向两极溶液中滴加酚酞试液,有一极溶液颜色变红,说明生成碱,则F为H2,可以确定A为NaCl,B为NaOH.由转化关系,可知H为NH3.常见金属X可与NaOH溶液反应生成H2,则X为Al,由转化关系可知,C为NaAlO2,D为AlCl3,I为Al(OH)3,据此解答.
解答:解:E、F、J在通常情况下是气体单质,E为有色气体,E为Cl2.J是空气中含量最多的气体,则J为N2.工业上常用电解A的饱和溶液的方法制取B,电解过程中,向两极溶液中滴加酚酞试液,有一极溶液颜色变红,说明生成碱,则F为H2,可以确定A为NaCl,B为NaOH.由转化关系,可知H为NH3.常见金属X可与NaOH溶液反应生成H2,则X为Al,由转化关系可知,C为NaAlO2,D为AlCl3,I为Al(OH)3,
(1)电解NaCl溶液的化学方程式为:2NaCl+2H2O
Cl2↑+H2↑+2NaOH,电解过程中,向两极溶液中滴加酚酞试液,有一极溶液颜色变红,该极有NaOH生成,氢离子发生还原反应生成氢气,则该极为阴极,该极的电极反应为 2H++2e-═H2↑,
故答案为:2NaCl+2H2O
Cl2↑+H2↑+2NaOH;阴;2H++2e-═H2↑;
(2)若将a mol AlCl3全部转化为NaAlO2,发生反应Al3++4OH-═2AlO2-+2H2O,则NaOH的物质的量的取值范围为n(NaOH)≥4amol,
故答案为:n(NaOH)≥4amol;
(3)H+D→I的离子方程式为:3NH3?H2O+Al3+═Al(OH)3↓+3NH4+;
B+X→C+F的离子方程式为:2Al+2H2O+2OH-═2AlO2-+3H2↑;
E与B溶液的反应离子方程式为:Cl2+2OH-═Cl-+ClO-+H2O,
故答案为:3NH3?H2O+Al3+═Al(OH)3↓+3NH4+;2Al+2H2O+2OH-═2AlO2-+3H2↑;
Cl2+2OH-═Cl-+ClO-+H2O.
(1)电解NaCl溶液的化学方程式为:2NaCl+2H2O
| ||
故答案为:2NaCl+2H2O
| ||
(2)若将a mol AlCl3全部转化为NaAlO2,发生反应Al3++4OH-═2AlO2-+2H2O,则NaOH的物质的量的取值范围为n(NaOH)≥4amol,
故答案为:n(NaOH)≥4amol;
(3)H+D→I的离子方程式为:3NH3?H2O+Al3+═Al(OH)3↓+3NH4+;
B+X→C+F的离子方程式为:2Al+2H2O+2OH-═2AlO2-+3H2↑;
E与B溶液的反应离子方程式为:Cl2+2OH-═Cl-+ClO-+H2O,
故答案为:3NH3?H2O+Al3+═Al(OH)3↓+3NH4+;2Al+2H2O+2OH-═2AlO2-+3H2↑;
Cl2+2OH-═Cl-+ClO-+H2O.
点评:本题考查无机物的推断,熟练掌握氯碱工业电解原理、金属Al的性质是关键,侧重对常用化学用语的考查,难度中等.

练习册系列答案
相关题目
(1)下列有关晶体的叙述中错误的是
A.石英晶体中的硅原子以sp2杂化方式与周围的氧原子形成共价键
B.氯化钠晶体中每个Na+或Cl-周围紧邻的有6个Cl-或Na+
C.在CsCl晶体中每个Cs+周围紧邻的有8个Cl-,而和每个Cl-等距离紧邻的也有8个Cs+
D.在面心立方密堆积的金属晶体中,每个金属原子周围紧邻的有4个金属原子
(2)已知MgO的晶体结构属于NaCl型.某同学画出的MgO晶胞结构示意图如图1所示,请改正图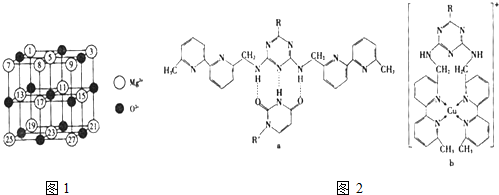
中错误: .(用文字表述)
(3)第三周期部分元素氟化物的熔点见下表:
解释表中氟化物熔点差异的原因: .
(4)人工模拟是当前研究的热点.有研究表明,化合物X可用于研究模拟酶,当其结合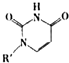 或Cu(I)(I表示化合价为+1)时,分别形成a和b:
或Cu(I)(I表示化合价为+1)时,分别形成a和b:
分析a和b中微粒间的相互作用(包括化学键和分子间相互作用)的差异,试指出
其不同点:a中含 ,b中含 .(用“氢键”、“配位键”、“极性键”、“非极性键”等填空)
A.石英晶体中的硅原子以sp2杂化方式与周围的氧原子形成共价键
B.氯化钠晶体中每个Na+或Cl-周围紧邻的有6个Cl-或Na+
C.在CsCl晶体中每个Cs+周围紧邻的有8个Cl-,而和每个Cl-等距离紧邻的也有8个Cs+
D.在面心立方密堆积的金属晶体中,每个金属原子周围紧邻的有4个金属原子
(2)已知MgO的晶体结构属于NaCl型.某同学画出的MgO晶胞结构示意图如图1所示,请改正图

中错误:
(3)第三周期部分元素氟化物的熔点见下表:
| 氟化物 | NaF | MgF2 | SiF4 |
| 熔点/K | 1266 | 1534 | 183 |
(4)人工模拟是当前研究的热点.有研究表明,化合物X可用于研究模拟酶,当其结合
 或Cu(I)(I表示化合价为+1)时,分别形成a和b:
或Cu(I)(I表示化合价为+1)时,分别形成a和b:分析a和b中微粒间的相互作用(包括化学键和分子间相互作用)的差异,试指出
其不同点:a中含




 它的空间利用率为
它的空间利用率为