题目内容
2.(1)浓硫酸与木炭在加热条件下反应的化学方程式是C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O.(2)试用如图所列各种装置设计一个实验;来验证上述反应所产生的各种产物.这些装置的连接顺序(按产生气体从左到右的方向)是④→②→①→③.(填装置的编号)

(3)实验时可观察到装置①中A瓶的溶液褪色,C瓶的溶液不褪色.A瓶溶液的作用是,B瓶溶液的作用是除去SO2.
(4)装置②所加的固体药品是无水CuSO4.
(5)装置③中所盛溶液是澄清石灰水.
分析 (1)浓硫酸与碳在加热条件下反应生成二氧化碳和二氧化硫和水,据此形成反应的化学方程式;
(2)检验二氧化碳和二氧化硫时用到的溶液中均含有水,所以先检验水的存在,二氧化碳和二氧化硫均可以使澄清石灰水变浑浊,所以先检验二氧化硫,再除去,最后检验二氧化碳;
(3)A瓶溶液的作用是证明有SO2;B中酸性KMnO4溶液作用是氧化二氧化硫;C中用到品红溶液作用是检验二氧化硫是否还存在;
(4)证明有水生成,利用无水硫酸铜遇水变蓝判断;
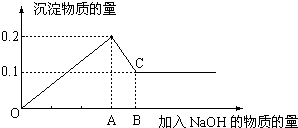
(5)装置③中氢氧化钙和二氧化碳反应生成白色沉淀,检验二氧化碳的存在.
解答 解:(1)浓硫酸与碳反应发生氧化还原反应,生成二氧化碳和二氧化硫和水,碳和稀硫酸不反应,反应的化学方程式为:C+2H2SO4(浓) $\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O,
故答案为:C+2H2SO4(浓) $\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O;
(2)木炭粉与浓硫酸发生反应选择固液加热装置选择④;检验二氧化碳和二氧化硫时用到的溶液中均含有水,所以先检验水的存在选择②;二氧化碳和二氧化硫均可以使澄清石灰水变浑浊,所以先检验二氧化硫,再除去,最后检验二氧化碳,选择①,尾气有毒需进行尾气处理选择③,
故答案为:④;②;①;③;
(3)二氧化硫具有漂泊性,能使品红褪色,A瓶溶液的作用是证明有SO2;B中酸性KMnO4溶液,作用是氧化二氧化硫,除去混合气体中的SO2,C中用到品红溶液作用是检验二氧化硫是否还存在,
故答案为:证明SO2的存在;除去SO2;
(4)实验利用白色硫酸铜遇到水变为蓝色证明含有水蒸气,
故答案为:无水CuSO4;
(5)因S02和C02都能使石灰水变浑浊,因此要想检验出C02,就要先检验S02,并除掉S02,这样石灰水变浑浊才能说明有C02,装置③是验证二氧化硫气体除净后,检验二氧化碳气体存在的实验装置,反应现象是二氧化碳和氢氧化钙反应生成白色沉淀,
故答案为:澄清石灰水.
点评 本题考查了浓硫酸性质应用,题目难度中等,注意理解浓硫酸的性质中和碳单质的反应原理,明确产物检验所用的试剂以及检验的先后顺序知识是解答的关键,综合性较强,充分考查了学生的分析、实验能力.

 同步练习强化拓展系列答案
同步练习强化拓展系列答案| A. | 原子半径:丁>丙>乙 | |
| B. | 甲的气态氢化物的水溶液呈酸性 | |
| C. | 乙与丙形成的化合物既能与酸反应,又能与碱反应 | |
| D. | 同周期元素中丁的最高价氧化物对应水化物的酸性最强 |
| A. | NH3溶于水后显碱性,在FeCl3饱和溶液中通入足量NH3可制取Fe(OH)3胶体 | |
| B. | 油脂在碱性条件下易水解,可用于制作肥皂 | |
| C. | 次氯酸钠具有强还原性,可用于配制“84”消毒液 | |
| D. | 铜的金属活动性比铝弱,可用铜罐代替铝罐贮运浓硝酸 |
| A. | 盐酸、硫酸 | B. | 氨水、氢氧化钠溶液 | ||
| C. | 氯化钠溶液、硫酸 | D. | 盐酸、氢氧化钠溶液 |
| A. | 轮船水线以下的船壳上装一定数量的锌块 | |
| B. | 铝片不用特殊方法保存 | |
| C. | 纯锌与稀硫酸反应时,滴入少量浓H2SO4溶液后速率加快 | |
| D. | 镀锌铁不如镀锡铁耐用 |
| A. | 工业上大量含硫燃料的燃烧 | B. | 工业生产使空气中CO2含量增加 | ||
| C. | SO2在尘埃催化下氧化为SO3 | D. | SO3与水反应生成H2SO4 |
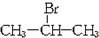 ,且烃A的结构简式为
,且烃A的结构简式为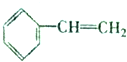 ,其在不同条件下能发生下图所示的一系列变化.
,其在不同条件下能发生下图所示的一系列变化.
 ,D
,D ,E
,E ,H
,H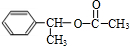 .
. +NaBr.
+NaBr. .
.