��Ŀ����
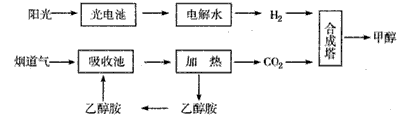
�ڸúϳ�·�߶��ڻ��������ļ�ֵ�����ܷ�ֹ����ЧӦ��
���Ҵ���(HOCH2CH2NH2)ˮ��Һ���������ԣ���ԭ��ɱ�ʾΪ
HOCH2CH2NH2+H2O
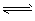 HOCH2CH2NH3++OH-;
HOCH2CH2NH3++OH-; ����CO2��H2�ϳ�CH3OH���Ȼ�ѧ����ʽ��CO2(g)+3H2(g)==CH3OH(l) +H2O(l) ��H=-131.9 kJ��mol-1
A������
B�����Т٢�
C�����Т٢ڢ�
D��ȫ����ȷ

 ��У����ϵ�д�
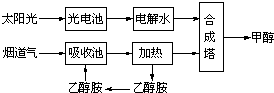
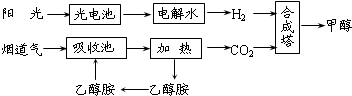
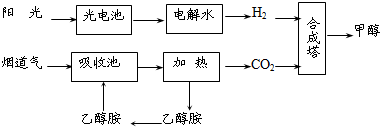
��У����ϵ�д���14�֣�����һ�������£���ѧ�����ô��̵����з����CO2��̫���ܵ�ص��ˮ������H2�ϳɼ״������������ͼ��ʾ���Իش��������⣺

(1)�úϳ�·�߶��ڻ��������ļ�ֵ���� ��
(2)15��20%���Ҵ�����HOCH2CH2NH2��ˮ��Һ���������ԣ������ϳ���·������CO2���ռ��������ӷ���ʽ��ʾ�Ҵ���ˮ��Һ�������Ե�ԭ�� ��
(3)CH3OH��H2��ȼ���ȷֱ�Ϊ����H����725.5kJ/mol����H����285.8kJ/mol��д����ҵ����CO2��H2�ϳ�CH3OH���Ȼ�ѧ����ʽ�� ��
��ȼú�����е�CO2ת��Ϊ���ѵķ�Ӧԭ��Ϊ��
2CO2(g) + 6H2(g) CH3OCH3(g)
+ 3H2O(g)
CH3OCH3(g)
+ 3H2O(g)
��֪һ��ѹǿ�£��÷�Ӧ�ڲ�ͬ�¶ȡ���ͬͶ�ϱ�ʱ��CO2��ת���ʼ��±���
|
Ͷ�ϱ�[n(H2) / n(CO2)] |
500 K |
600 K |
700 K |
800 K |
|
1.5 |
45% |
33% |
20% |
12% |
|
2.0 |
60% |
43% |
28% |
15% |
|
3.0 |
83% |
62% |
37% |
22% |
(4)�÷�Ӧ���ʱ���H 0���ر���S___0�����������
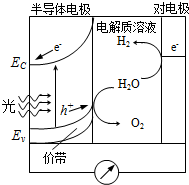
(5)�ü�����Ϊȼ�ϵ��ԭ�ϣ��ڼ��Խ����иõ�ظ����ĵ缫��Ӧʽ ������1.12 L��min-1����״������������õ����ͨ����ѣ��е�Ϊ-24.9 �棩���øõ�ص��500 mL 2 mol��L-1 CuSO4��Һ��ͨ��0.50 min�������Ͽ���������ͭ g��