��Ŀ����
��1����CO2ת�����л������Чʵ��̼ѭ�����磺
��6CO2+6H2O
C6H12O6+6O2
��CO2+CH4
CH3COOH
��2CO2+6H2
CH2=CH2+4H2O
�����Ϸ�Ӧ����������ȷ����
A������ܵ��Ƿ�Ӧ��
B����Ӧ�ڵ�ԭ��������Ϊ100%
C����Ӧ���е����ַ�Ӧ�ﶼ�ǿ���������Ȼ����
D����Ӧ����Ŀǰ��ҵ������ϩ������Ҫ����
��2����һ�������£���ѧ�����ô��̵����з����CO2��̫���ܵ�ص��ˮ������H2�ϳɼ״����������ͼ��ʾ���Իش��������⣺
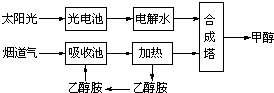
��15��20%���Ҵ�����HOCH2CH2NH2��ˮ��Һ���������ԣ���NH3����ˮ��ԭ�����ƣ��������ϳ���·������CO2���ռ��������ӷ���ʽ��ʾ�Ҵ���ˮ��Һ�������Ե�ԭ��
��CH3OH��l����H2��g����ȼ���ȷֱ�Ϊ����H=-725.5kJ?mol-1����H=-285.8kJ?mol-1��д����ҵ����CO2��g����H2��g���ϳ�CH3OH��l�����Ȼ�ѧ����ʽ��
�۾ݱ�������300�桢70MPa���ɶ�����̼�������ϳ��Ҵ�Ҳ�ѳ�Ϊ��ʵ��2CO2��g��+6H2��g��?CH3CH2OH��g��+3H2O��g�����÷�Ӧ�ġ�S
��6CO2+6H2O
| ������� |
��CO2+CH4
| ���� |
| �� |
��2CO2+6H2
| ���� |
| �� |
�����Ϸ�Ӧ����������ȷ����
AB
AB
��������ţ�A������ܵ��Ƿ�Ӧ��
B����Ӧ�ڵ�ԭ��������Ϊ100%
C����Ӧ���е����ַ�Ӧ�ﶼ�ǿ���������Ȼ����
D����Ӧ����Ŀǰ��ҵ������ϩ������Ҫ����
��2����һ�������£���ѧ�����ô��̵����з����CO2��̫���ܵ�ص��ˮ������H2�ϳɼ״����������ͼ��ʾ���Իش��������⣺

��15��20%���Ҵ�����HOCH2CH2NH2��ˮ��Һ���������ԣ���NH3����ˮ��ԭ�����ƣ��������ϳ���·������CO2���ռ��������ӷ���ʽ��ʾ�Ҵ���ˮ��Һ�������Ե�ԭ��
HOCH2CH2NH2+H2O?HOCH2CH2NH3++OH-
HOCH2CH2NH2+H2O?HOCH2CH2NH3++OH-
����CH3OH��l����H2��g����ȼ���ȷֱ�Ϊ����H=-725.5kJ?mol-1����H=-285.8kJ?mol-1��д����ҵ����CO2��g����H2��g���ϳ�CH3OH��l�����Ȼ�ѧ����ʽ��
CO2��g��+3H2��g���TCH3OH��l��+H2O��l������H=-131.9KJ/mol
CO2��g��+3H2��g���TCH3OH��l��+H2O��l������H=-131.9KJ/mol
���۾ݱ�������300�桢70MPa���ɶ�����̼�������ϳ��Ҵ�Ҳ�ѳ�Ϊ��ʵ��2CO2��g��+6H2��g��?CH3CH2OH��g��+3H2O��g�����÷�Ӧ�ġ�S
��
��
�����������=��������0�����ݷ�Ӧ���Է����У��Ƶø÷�Ӧ�ġ�H��
��
�����������=��������0����������1��A�����ݢ��ǹ���ת��Ϊ��ѧ�ܣ�������Ӧ������ת��ɻ�ѧ�ܣ�
B��ԭ��������Ϊ100%�ķ�Ӧ�Ƿ�Ӧ��ȫ��ת��Ϊ�����
C������CO2������Ȼ���ʣ�
D����ҵ����Ҫͨ��ʯ���ѽ�ķ����Ʊ���ϩ��
��2���ٰ������ˮ����ƽ���е������ӣ��ٽ�ˮ����ƽ��������У�����������Ũ��������Һ�Լ��ԣ�
�����ø�˹���ɼ��㷴Ӧ�ȣ�����д�Ȼ�ѧ����ʽ��
����ָ������ϵ�Ļ��ҵij̶ȣ���Ӧ�Է�����˵����H-T��S��0��
B��ԭ��������Ϊ100%�ķ�Ӧ�Ƿ�Ӧ��ȫ��ת��Ϊ�����
C������CO2������Ȼ���ʣ�
D����ҵ����Ҫͨ��ʯ���ѽ�ķ����Ʊ���ϩ��
��2���ٰ������ˮ����ƽ���е������ӣ��ٽ�ˮ����ƽ��������У�����������Ũ��������Һ�Լ��ԣ�
�����ø�˹���ɼ��㷴Ӧ�ȣ�����д�Ȼ�ѧ����ʽ��
����ָ������ϵ�Ļ��ҵij̶ȣ���Ӧ�Է�����˵����H-T��S��0��
����⣺��1��A�����ǹ���ת��Ϊ��ѧ�ܣ�������Ӧ������ת��ɻ�ѧ�ܣ���������ܵ��Ƿ�Ӧ�٣���A��ȷ��
B��ԭ��������Ϊ100%�ķ�Ӧ�Ƿ�Ӧ��ȫ��ת��Ϊ�������B��ȷ��
C��CO2������Ȼ���ʣ�CH4�ǿ���������Ȼ���ʣ���C����
D���ѽ�������ѻ����Ի�ö���������������ҪΪ��ϩ����ϩ������ϩ�ȣ�Ϊ��Ҫ�ɷֵ�ʯ�ͼӹ����̣���D����
��ѡAB��
��2�����Ҵ���ˮ��Һ����������ȡ����������������ӣ�ʹ��Һ�е�����������Ũ������Ӧ�����ӷ���ʽΪ��HOCH2CH2NH2+H2O?HOCH2CH2NH3++OH-���ʴ�Ϊ��HOCH2CH2NH2+H2O?HOCH2CH2NH3++OH-��
�ڼ״���������ȼ������д���Ȼ�ѧ����ʽ�ֱ�Ϊ��
��2CH3OH��l��+3O2��g��=2CO2��g��+4H2O��l������H1=-1451kJ/mol��
��2H2��g��+O2��g��=2H2O��l������H2=-571.6KJ/mol��
���ݸ�˹���ɣ���ӦCO2��g��+3H2��g���TCH3OH��l��+H2O��l��
���Կ����Ƿ���ʽ
����-�١�
�����ԡ�H=��
��-571.6KJ/mol��-��-1451kJ/mol����
=-131.9KJ/mol��
�ʴ�Ϊ��CO2��g��+3H2��g���TCH3OH��l��+H2O��l������H=-131.9KJ/mol��
�۷�Ӧ����8mol����������4mol���ʡ�SС��0����Ӧ�Է�����˵����H-T��S��0���ʡ�H��0���ʴ�Ϊ����������
B��ԭ��������Ϊ100%�ķ�Ӧ�Ƿ�Ӧ��ȫ��ת��Ϊ�������B��ȷ��
C��CO2������Ȼ���ʣ�CH4�ǿ���������Ȼ���ʣ���C����
D���ѽ�������ѻ����Ի�ö���������������ҪΪ��ϩ����ϩ������ϩ�ȣ�Ϊ��Ҫ�ɷֵ�ʯ�ͼӹ����̣���D����
��ѡAB��
��2�����Ҵ���ˮ��Һ����������ȡ����������������ӣ�ʹ��Һ�е�����������Ũ������Ӧ�����ӷ���ʽΪ��HOCH2CH2NH2+H2O?HOCH2CH2NH3++OH-���ʴ�Ϊ��HOCH2CH2NH2+H2O?HOCH2CH2NH3++OH-��
�ڼ״���������ȼ������д���Ȼ�ѧ����ʽ�ֱ�Ϊ��
��2CH3OH��l��+3O2��g��=2CO2��g��+4H2O��l������H1=-1451kJ/mol��
��2H2��g��+O2��g��=2H2O��l������H2=-571.6KJ/mol��
���ݸ�˹���ɣ���ӦCO2��g��+3H2��g���TCH3OH��l��+H2O��l��
���Կ����Ƿ���ʽ
| 3 |
| 2 |
| 1 |
| 2 |
| 3 |
| 2 |
| 1 |
| 2 |
�ʴ�Ϊ��CO2��g��+3H2��g���TCH3OH��l��+H2O��l������H=-131.9KJ/mol��
�۷�Ӧ����8mol����������4mol���ʡ�SС��0����Ӧ�Է�����˵����H-T��S��0���ʡ�H��0���ʴ�Ϊ����������
���������⿼����ɫ��ѧ��ȼ���ȸ������Ӧ�ã���Ŀ�Ѷ��еȣ�ע�ⷴӦ�Է�����˵����H-T��S��0��

��ϰ��ϵ�д�
 ��ĩ���䵥Ԫ�����ิϰ��ϵ�д�
��ĩ���䵥Ԫ�����ิϰ��ϵ�д�
�����Ŀ
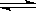 Sr2+��aq��+SO2-4��aq��KSP=2.5��10-7
Sr2+��aq��+SO2-4��aq��KSP=2.5��10-7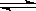 Sr2+��aq��+SO2-4��aq��KSP=
Sr2+��aq��+SO2-4��aq��KSP= 2.5��10-7
2.5��10-7 �۽��ͣ�
�۽��ͣ� Һ��ʵ���м���SO2-4�ij����Լ���ij��ѧ�о���ѧϰС�����ij��Һ�д���SO2-4ʱ�����ȼ���Ba��NO3��2��Һ��������ɫ������Ȼ��������ϡ���ᣬ��ɫ�������ܽ⣬�ɴ˵ó����ۣ���Һ��һ������SO2-4��
Һ��ʵ���м���SO2-4�ij����Լ���ij��ѧ�о���ѧϰС�����ij��Һ�д���SO2-4ʱ�����ȼ���Ba��NO3��2��Һ��������ɫ������Ȼ��������ϡ���ᣬ��ɫ�������ܽ⣬�ɴ˵ó����ۣ���Һ��һ������SO2-4��