��Ŀ����
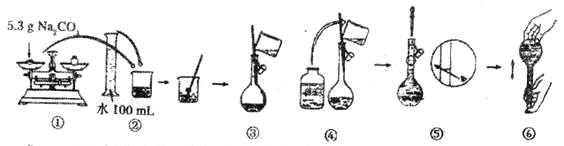
����Ŀ��������������Fe3O4�������������ȶ���������������;�㷺�����ٴ���ϡ����\���ͻ�����ѧ�ȶ������DZ��Ӧ�õ��������ߡ�ˮ�ȷ��Ʊ�Fe3O4�������ķ�Ӧ��
3Fe2��2S2O![]() ��O2��xOH��
��O2��xOH��![]() Fe3O4����S4O
Fe3O4����S4O![]() ��2H2O��
��2H2O��
��ش��������⣺
��1��ˮ�ȷ��Ʊ�Fe3O4�������ķ�Ӧ�У���ԭ����__________________��S2O![]() ��S�Ļ��ϼ�Ϊ________________.
��S�Ļ��ϼ�Ϊ________________.
��2����Ӧ�Ļ�ѧ����ʽ��![]() =____________.
=____________.
��3��ÿ���� 1mol Fe3O4����Ӧת�Ƶĵ���Ϊ_________mol����Fe2����ԭ��O2�����ʵ���Ϊ________mol.
���𰸡���1��Fe2����S2O32������2 ��2��4 ��3��4 0.5
��������
�����������1��ˮ�ȷ��Ʊ�Fe3O4�������ķ�Ӧ�У���Ԫ�صĻ��ϼ۴ӣ�2�۲������ߵ���3�ۣ�������Ԫ�صĻ��ϼ۴ӣ�2�����ߵ���2.5�ۣ���ʧȥ���ӣ����Ի�ԭ����Fe2����S2O32����S2O![]() ��S�Ļ��ϼ�Ϊ��2�ۣ�
��S�Ļ��ϼ�Ϊ��2�ۣ�
��2��������ԭ���غ��֪��Ӧ�Ļ�ѧ����ʽ��x=4��
��3��ÿ���� 1mol Fe3O4������1mol��������˷�Ӧת�Ƶĵ���Ϊ4mol��3mol������������2mol�ǻ�ԭ����ʧȥ2mol���ӣ���˸��ݵ��ӵ�ʧ�غ��֪��Fe2����ԭ��O2�����ʵ���Ϊ0.5mol��