题目内容
【题目】某原电池装置如下图所示,电池总反应为2Ag+Cl2==="2AgCl" 。下列说法正确的是
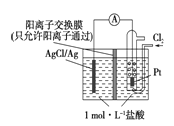
A. 正极反应为AgCl+e-===Ag+Cl-
B. 放电时,交换膜右侧溶液中有大量白色沉淀生成
C. 若用NaCl溶液代替盐酸,则电池总反应随之改变
D. 当电路中转移0.01 mol e-时,交换膜左侧溶液中约减少0.02 mol离子
【答案】D
【解析】试题分析:A、正极反应式为Cl2+2e-=2Cl-,A项错误;B、由于阳离子交换膜只允许阳离子通过,故在左侧溶液中才会有大量白色沉淀生成,B项错误;C、若用NaCl溶液代替盐酸,但电池总反应不变,C项错误;D、当电路中转移0.01 mol e-时,交换膜左侧产生0.01 mol Ag+与盐酸反应产生AgCl沉淀,同时约有0.01 mol H+通过阳离子交换膜转移到右侧溶液中,故左侧溶液共约0.02 mol离子减少,D项正确;答案选D。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目