题目内容
等体积、等物质的量浓度的盐酸、氢氧化钠溶液分别放在甲、乙两烧杯中,各加等质量的铝,生成氢气的体积比为5∶7,则甲、乙两烧杯中的反应情况可能分别是
| A.甲、乙中都是铝过量 |
| B.甲中铝过量,乙中碱过量 |
| C.甲中酸过量,乙中铝过量 |
| D.甲中酸过量,乙中碱过量 |
B
解析试题分析:铝与盐酸和氢氧化钠溶液反应的离子方程式分别为2Al+6H+=2Al3++3H2↑、2Al+2OH-+2H2O=2AlO2-+3H2↑。因此如果铝全部反应,则生成的氢气体积相等。由于消耗等物质的量的铝时,消耗盐酸的物质的量大于消耗氢氧化钠的物质的量,所以在盐酸和氢氧化钠的物质的量相等的条件下,如果反应中生成氢气的体积比为5∶7,则甲中盐酸不足,铝过量。而乙中氢氧化钠过量,铝不足,因此正确的答案选B。
考点:考查铝与盐酸和氢氧化钠溶液反应的计算

练习册系列答案
相关题目
一定条件下,将Na与O2反应的生成物1.5g溶于水,所得溶液恰好能被80mL浓度为0.5 mol·L—1的HCl溶液中和,则该生成物的成分是
| A.Na2O | B.Na2O2 | C.Na2O和Na2O2 | D.Na2O2和NaO2 |
下列说法不正确的是
| A.用坩埚钳夹住一小块铝箔在酒精灯上加热到熔化,但熔化的铝并不滴落,是因为铝表面生成了熔点更高的氧化铝。 |
| B.铜属于重金属,它的化学性质不活泼,铜盐有毒,能使蛋白质失去活性,故误食铜盐后,应立即服用牛奶或蛋清急救再送医院治疗。 |
C.盐桥中通常装有琼脂的KCl溶液,形成如图所示原电池的闭合回路时,氯离子向正极移动,钾离子向负极移动。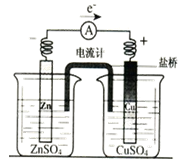 |
| D.水的电离是吸热反应,升高温度,促进水的电离,水的离子积常数Kw变大。 |
中科院化学所研制的晶体材料——纳米四氧化三铁,在核磁共振造影及医药上有广泛用途其生产过程的部分流程如下图所示。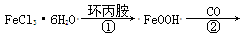 纳米四氧化三铁。下列有关叙述不合理的是
纳米四氧化三铁。下列有关叙述不合理的是
| A.纳米四氧化三铁可分散在水中,它与FeCl3溶液的分散质直径相当 |
| B.纳米四氧化三铁具有磁性,可作为药物载体用于治疗疾病 |
| C.在反应①中环丙胺的作用可能是促进氯化铁水解 |
| D.反应②的化学方程式是6FeOOH+CO=2Fe3O4+3H2O十CO2 |
要除去FeCl2溶液中的少量氯化铁,可行的办法( )
| A.加入KSCN溶液 | B.通入氯气 |
| C.加入NaOH 溶液 | D.加入铁粉 |
信息时代产生的大量电子垃圾对环境构成了极大的威胁。某“变废为宝”学生探究小组将一批废弃的线路板简单处理后,得到含70% Cu、25% Al、4% Fe及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜和硫酸铝晶体的路线:
下列关于第①步的说法,错误的是
| A.Al起始反应的离子方程式为2Al + 6H+ = 2Al3+ + 3H2↑ |
| B.滤液I中一定含有Cu2+、Al3+;一定含有Fe2+和Fe3+中的一种或两种 |
| C.滤渣I的主要成分是Au与Pt,由此可以回收贵重的金属 |
| D.加入稀硫酸可以提高硝酸的利用率,使硝酸根离子完全反应 |
下列物质间的转化不能通过一步化合反应实现的是
| A.Fe→FeCl3 | B.AlCl3→Al(OH)3 |
| C.Fe→FeCl2 | D.Na2O→NaOH |
把2.1g的CO与H2组成的混合气体与足量的O2充分燃烧后,立即通入足量的Na2O2固体中,固体的质量增加
| A.7.2g | B.3.6g | C.2.1 | D.无法确定 |
关于Na2CO3和NaHCO3性质的说法正确的是
| A.等浓度时水溶液碱性:NaHCO3>Na2CO3 |
| B.热稳定性:NaHCO3>Na2CO3 |
| C.与盐酸溶液反应的速率(快慢):NaHCO3<Na2CO3 |
| D.向饱和 Na2CO3溶液中通入过量CO2,有晶体析出 |