题目内容
【题目】物质甲是一种重要的有机化工原料,其结构简式为![]() ,它一般不可能具有的性质是
,它一般不可能具有的性质是
A. 易溶于水,不易溶于有机溶剂
B. 在空气中燃烧产生黑烟
C. 能使溴的四氯化碳溶液褪色
D. 能发生加成反应在一定条件下可与4倍物质的量的氢气加成
【答案】A
【解析】试题分析:A.因为物质甲为烃,所以物质甲难溶于水,易溶于有机溶剂,A项符合题意;B.物质甲的分子式为C8H8,含碳量很高,所以在空气中燃烧产生黑烟,B项不符合题意;C.因为分子中含碳碳双键,所以能与Br2发生加成反应,即能使溴的四氯化碳溶液褪色,C项不符合题意;D.1mol苯环能与3molH2发生加成反应,1mol碳碳双键能与1molH2发生加成反应,则一定条件下可与4倍物质的量的氢气加成,D项不符合题意;答案选A。

 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案【题目】硫代硫酸钠俗称保险粉,可用于照相业作定影剂、纸浆漂白作脱氯剂等。实验室用SO2通入Na2S和Na2CO3的混合溶液中来制备硫代硫酸钠。本实验对Na2S纯度要求较高,利用项图所示的装置可将工业级的Na2S提纯。已知Na2S常温下微溶于酒精,加热时溶解度迅速增大,杂质不溶于酒精。提纯过程为:将已称量好的工业级Na2S放入圆底烧瓶中,加入一定质量的酒精和少量水。按下图所示装配所需仪器,向冷凝管通入冷却水,同时水浴加热。待烧瓶中固体不再减少时,停止加热。将烧瓶取下,立即趁热过滤,再冷却结晶,过滤。将所得固体洗涤、干燥,得到Na2S9H2O晶体。

(1)下列说法不正确的是______。
A.将晶体转移至布氏漏斗时,若器壁上粘有少量晶体,应用冷水淋洗
B.抽滤时,为防止滤纸穿孔,可适当关小水龙头或多加一层滤纸
C.洗涤时,可用一定浓度的乙醇溶液洗涤晶体,目的是洗除晶体表面的杂质,易于得到干燥晶体
D.为加快产品的干燥,可高温烘干
E.在提纯过程中“趁热过滤”操作的目的是防止硫化钠结晶析岀而损失、去除杂质
(2)用下图所示装置制取Na2S2O3,其中盛放Na2SO3固体的玻璃仪器名称是______,三颈烧瓶中发生反应的化学方程式______。

(3)保险粉样品中Na2S2O35H2O的纯度(质量分数)可通过氧化还原滴定法测定,相关反应方程式为2Na2S2O3+I2=2NaI+Na2S4O6,准确称取Wg样品于锥形瓶中,用适量蒸馏水溶解,并滴加淀粉溶液作指示剂。用0.1000mol/L碘的标准溶液进行滴定。请回答:
①到达滴定终点的标志______;
②滴定起始和终点的液面位置如图,则消耗碘的标准溶液体积为______,产品的纯度为______(设Na2S2O35H2O相对分子质量为M)。

③若滴定时振荡不充分,刚看到溶液局部变色就停止滴定,则会使样品中Na2S2O35H2O的纯度的测量结果______(“偏高”、“偏低”或“不变”)。
(4)某研究小组以硫代硫酸钠与硫酸反应来探究外界条件对反应速率的影响,设计实验如下:
实验 编号 | 实验温度 /℃ | Na2S2O3 | H2SO4 | 蒸馏水体积 /mL | ||
体积/mL | 浓度/mol/L | 体积/mL | 浓度/mol/L | |||
① | 25 | 10 | 0.1 | 10 | 0.1 | 0 |
② | 25 | 5 | 0.1 | 10 | 0.1 | 5 |
③ | 25 | 5 | 0.2 | 10 | 0.2 | 5 |
④ | 50 | 5 | 0.1 | 10 | 0.1 | 5 |
⑤ | 50 | 10 | 0.2 | 5 | 0.2 | 5 |
下列有关说法不正确的是______。
A.该同学在实验中采用的研究方法是实验比较法
B.实验①和②探究其他条件不变时Na2S2O3浓度对相关反应速率的影响
C. 实验①和③溶液变浑浊的时间相同
D.其他条件不变时,探究温度对化学反应速率的影响,应选择实验③和实验⑤
【题目】苯乙酸铜是合成优良催化剂、传感材料——纳米氧化铜的重要前驱体之一。下面是它的一种实验室合成路线:
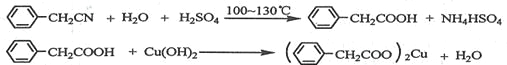
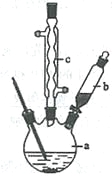
制备苯乙酸的装置示意图如下(加热和夹持装置等略):
已知:苯乙酸的熔点为76.5 ℃,微溶于冷水,溶于乙醇。
回答下列问题:
(1)在250 mL三口瓶a中加入70 mL70%硫酸。配制此硫酸时,加入蒸馏水与浓硫酸的先后顺序是
__________________________。
(2)将a中的溶液加热至100 ℃,缓缓滴加40 g苯乙腈到硫酸溶液中,然后升温至130 ℃继续反应。在装置中,仪器b的作用是_____________________;仪器c的名称是______________,其作用是___________________________________________。
反应结束后加适量冷水,再分离出苯乙酸粗品。加人冷水的目的是____________。下列仪器中可用于分离苯乙酸粗品的是________________(填标号)。
A.分液漏斗 | B.漏斗 | C.烧杯 | D.直形冷凝管E.玻璃棒 |
(3)提纯粗苯乙酸的方法是_____________,最终得到44 g纯品,则苯乙酸的产率是________。
(4)用CuCl2 2H2O和NaOH溶液制备适量Cu(OH)2沉淀,并多次用蒸馏水洗涤沉淀,判断沉淀洗干净的实验操作和现象是____________________________________________。
(5)将苯乙酸加人到乙醇与水的混合溶剂中,充分溶解后,加入Cu(OH)2搅拌30min,过滤,滤液静置一段时间,析出苯乙酸铜晶体,混合溶剂中乙醇的作用是___________________。
【题目】对硝基甲苯是医药、染料等工业的一种重要有机中间体,它常以浓硝酸为硝化剂,浓硫酸为催化剂,通过甲苯的硝化反应制备。

一种新的制备对硝基甲苯的实验方法是:以发烟硝酸为硝化剂,固体NaHSO4为催化剂(可循环使用),在CCl4溶液中,加入乙酸酐(有脱水作用),45℃反应1h 。反应结束后,过滤,滤液分别用5% NaHCO3溶液、水洗至中性,再经分离提纯得到对硝基甲苯。
(1)上述实验中过滤的目的是________________________。
(2)滤液在分液漏斗中洗涤静置后,有机层处于______层(填“上”或'下”);放液时,若发现液体流不下来,其可能原因除分液漏斗活塞堵塞外,还有_______________。
(3)下列给出了催化剂种类及用量对甲苯硝化反应影响的实验结果。
催化剂 | n(催化剂) | 硝化产物中各种异构体质量分数(%) | 总产率(%) | ||
对硝基甲苯 | 邻硝基甲苯 | 间硝基甲苯 | |||
浓H2SO4 | 1.0 | 35.6 | 60.2 | 4.2 | 98.0 |
1.2 | 36.5 | 59.5 | 4.0 | 99.8 | |
NaHSO4 | 0.15 | 44.6 | 55.1 | 0.3 | 98.9 |
0.25 | 46.3 | 52.8 | 0.9 | 99.9 | |
0.32 | 47.9 | 51.8 | 0.3 | 99.9 | |
0.36 | 45.2 | 54.2 | 0.6 | 99.9 | |
①NaHSO4催化制备对硝基甲苯时,催化剂与甲苯的最佳物质的量之比为______________。
②由甲苯硝化得到的各种产物的含量可知,甲苯硝化反应的特点是___________________。
③与浓硫酸催化甲苯硝化相比,NaHSO4催化甲苯硝化的优点有____________。
【题目】以氯化钾和钛白厂的副产品硫酸亚铁为原料生产硫酸钾、过二硫酸铵和氧化铁红颜料, 原料的综合利用率较高。其主要流程如下:

(1)反应I前需在FeSO4溶液中加入_____(填字母),以除去溶液中的Fe3+。
A.锌粉 | B.铁屑 | C.KI溶液 | D.H2 |
(2)反应I需控制反应温度低35℃,其目的是______________________。
(3)工业生产上常在反应Ⅲ的过程中加入一定量的醇类溶剂,其目的是:________。
(4)反应Ⅳ常被用于电解生产(NH4)2S2O8(过二硫酸铵)。电解时均用惰性电极,阳极
发生的电极反应可表示为:__________________________。




