题目内容
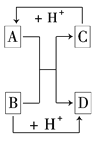
【题目】已知硅及其化合物之间存在如图转化关系。其中A是制造芯片和光电池的主要原料;B是含硅化合物中的一种气体;某些C可作干燥剂或催化剂的载体;D是一种黏合剂,能将磨砂玻璃黏合在一起,E是一种比H2CO3酸性还弱的酸。

试回答下列问题:
(1)写出A、C、E的化学式:A________、C________、E________。
(2)①~⑦反应中,属于氧化还原反应的是________,属于置换反应的是______,属于离子反应的是________。
【答案】Si SiO2 H2SiO3 ①③④ ①④ ④⑤⑥
【解析】
解题流程:

①~⑦反应分别是:
①Si+4HF===SiF4↑+2H2↑。是氧化还原反应,也是置换反应,不是离子反应(氢氟酸是弱酸,在溶液中HF的电离微弱,不能拆为离子形式);
②SiO2+4HF===SiF4↑+2H2O。不是氧化还原反应,不是置换反应,也不是离子反应;
③Si+O2===SiO2是氧化还原反应,不是置换反应,也不是离子反应;
④Si+2NaOH+H2O===Na2SiO3+2H2↑(Si+2OH+H2O===SiO32-+2H2↑)。是氧化还原反应,是置换反应(有单质和化合物参加,也有单质和化合物生成),也是离子反应;
⑤2NaOH+SiO2===Na2SiO3+H2O(2OH+SiO2=== SiO32-+H2O)。不是氧化还原反应,也不是置换反应,是离子反应;
⑥Na2SiO3+2HCl===2NaCl+H2SiO3↓(SiO32-+2H+===H2SiO3↓)。不是氧化还原反应,也不是置换反应,是离子反应;
⑦H2SiO3![]() H2O+SiO2。不是氧化还原反应,不是置换反应,也不是离子反应。
H2O+SiO2。不是氧化还原反应,不是置换反应,也不是离子反应。
综合以上分析,①~⑦反应中,属于氧化还原反应的是①③④,属于置换反应的是①④,属于离子反应的是④⑤⑥。

 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案【题目】I.CO、CO2的应用和治理是当今社会的热点问题。
CO工业上可用于高炉炼铁,发生如下反应: 1/3Fe2O3(s) + CO(g)![]() 2/3Fe(s) + CO2(g),已知该反应在不同温度下的平衡常数如下表:
2/3Fe(s) + CO2(g),已知该反应在不同温度下的平衡常数如下表:
温度/℃ | 1000 | 1150 | 1300 |
平衡常数 | 4.0 | 3.7 | 3.5 |
(1)该反应的正反应为_____反应(填“放热”或“吸热”),欲提高CO的平衡转化率,促进Fe2O3的转化,可采取的措施是____(选填序号)
a.及时吸收或移出CO2 b.增大反应体系的压强
c.用更高效的催化剂 d.粉碎矿石,增大接触面积
(2)一定条件下,在容积一定的容器中,铁和CO2发生反应:Fe(s)+CO2(g)![]() FeO(s)+CO(g)-Q,该反应的平衡常数表达式K=_____________。下列措施中能使平衡时
FeO(s)+CO(g)-Q,该反应的平衡常数表达式K=_____________。下列措施中能使平衡时![]() 增大的是______(选填编号)。
增大的是______(选填编号)。
a.升高温度 b.增大压强
c.充入一定量CO d.再加入一些铁粉
II.合成尿素的反应为:2NH3(g)+CO2(g) ![]() CO(NH2)2(s)+H2O(g)+Q(Q>0)。
CO(NH2)2(s)+H2O(g)+Q(Q>0)。
一定条件下,在10 L的恒容密闭容器中,充入2 mol NH3和1 mol CO2,反应经5 min后达到平衡,测得容器中CO2的浓度为0.05molL-1 。
完成下列填空:
(1)平均反应速率υ(NH3)=____________。
(2)下列描述中能说明上述反应已达平衡的是_________。(填序号)
a.2υ正(NH3)=υ逆(H2O) b.气体的平均相对分子质量不随时间而变化
c.NH3和CO2的比例保持不变 d.气体的压强不再发生变化
(3)为提高尿素的产率,工业上用该反应生产尿素时,合适的反应条件是_______。(填序号)
a.200℃ b.800℃ c.101 kPa d.24000 kPa