题目内容
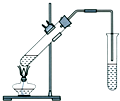 “酒是陈年的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们可以用如图所示的装置由乙醇、乙酸和浓硫酸来制取乙酸乙酯.回答下列问题:
“酒是陈年的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们可以用如图所示的装置由乙醇、乙酸和浓硫酸来制取乙酸乙酯.回答下列问题:(1)配制混合液时,加入试剂的正确顺序是
A.先加入乙醇,再慢慢注入浓硫酸和乙酸
B.先加入浓硫酸,再慢慢注入乙醇和乙酸
(2)在装置中乙试管常加入
A.NaOH溶液B.饱和Na2CO3溶液 C.NaCl溶液 D.CuSO4溶液
(3)若要将乙试管中的乙酸乙酯分离出来,应采用的实验操作是
(4)写出制取乙酸乙酯反应的化学方程式
分析:(1)类比浓硫酸的稀释进行判断;
(2)制备乙酸乙酯时常用饱和碳酸钠溶液吸收乙酸乙酯,乙醇溶解,碳酸钠与乙酸反应除去乙酸、同时降低乙酸乙酯的溶解度,便于分层;
(3)分离互不相溶的液体,可用分液的方法分离;
(4)乙酸与乙醇在浓硫酸作用下加热发生酯化反应生成乙酸乙酯和水,该反应为可逆反应.
(2)制备乙酸乙酯时常用饱和碳酸钠溶液吸收乙酸乙酯,乙醇溶解,碳酸钠与乙酸反应除去乙酸、同时降低乙酸乙酯的溶解度,便于分层;
(3)分离互不相溶的液体,可用分液的方法分离;
(4)乙酸与乙醇在浓硫酸作用下加热发生酯化反应生成乙酸乙酯和水,该反应为可逆反应.
解答:解:(1)浓硫酸的稀释是将浓硫酸加入水中,边加边搅拌,迁移到此处,即将浓硫酸加入到乙醇中,边摇动试管边慢慢加入浓硫酸和醋酸,所以正确是A,
故选A;
(2)制备乙酸乙酯时常用饱和碳酸钠溶液吸收乙酸乙酯,目的是除去乙醇和乙酸、降低乙酸乙酯的溶解度,便于分层,所以B正确,
故选B;
(3)分离乙酸乙酯时先将盛有混合物的试管充分振荡,让饱和碳酸钠溶液中和挥发出来的乙酸,使之转化为乙酸钠溶于水中,溶解挥发出来的乙醇;降低乙酸乙酯在水中的溶解度,静置分层后取上层得乙酸乙酯,
故答案为:分液;
(4)乙酸与乙醇在浓硫酸作用下加热发生酯化反应生成乙酸乙酯和水,同时该反应可逆,反应的化学方程式为:CH3COOH+CH3CH2OH
CH3COOC2H5+H2O,
故答案为:CH3COOH+CH3CH2OH
CH3COOC2H5+H2O.
故选A;
(2)制备乙酸乙酯时常用饱和碳酸钠溶液吸收乙酸乙酯,目的是除去乙醇和乙酸、降低乙酸乙酯的溶解度,便于分层,所以B正确,
故选B;
(3)分离乙酸乙酯时先将盛有混合物的试管充分振荡,让饱和碳酸钠溶液中和挥发出来的乙酸,使之转化为乙酸钠溶于水中,溶解挥发出来的乙醇;降低乙酸乙酯在水中的溶解度,静置分层后取上层得乙酸乙酯,
故答案为:分液;
(4)乙酸与乙醇在浓硫酸作用下加热发生酯化反应生成乙酸乙酯和水,同时该反应可逆,反应的化学方程式为:CH3COOH+CH3CH2OH
| 浓硫酸 |
| △ |
故答案为:CH3COOH+CH3CH2OH
| 浓硫酸 |
| △ |
点评:本题考查乙酸乙酯的制备,注意实验混合液的配制、饱和碳酸钠溶液的作用以及酯化反应的机理,本题难度中等.

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目
(每空2分,16分)生活中的有机物种类丰富,在衣食住行等多方面应用广泛,其中乙醇是比较常见的有机物。
(1)乙醇是无色有特殊香味的液体,密度比水_________。
(2)工业上用乙烯与水反应可制得乙醇,该反应的化学方程式为________________ (不用写反应条件),原子利用率是_________ 。
(3)下列属于乙醇的同系物的是_____,属于乙醇的同分异构体的是_____。(选填编号)
(4)乙醇能够发生氧化反应:
① 46 g乙醇完全燃烧消耗__________mol氧气。
②乙醇在铜做催化剂的条件下可被氧气氧化为乙醛,反应的化学方程式为_____________。
③下列说法正确的是__________。(选填字母)
| A.乙醇不能和酸性高锰酸钾溶液发生氧化还原反应 |
| B.交警用橙色的酸性重铬酸钾溶液检查司机是否酒后驾车 |
| C.黄酒中某些微生物使乙醇氧化为乙酸,于是酒就变酸了 |
| D.陈年的酒很香是因为乙醇和乙醇被氧化生成的乙酸发生酯化反应生成了乙酸乙酯 |

