题目内容
3.根据下列实验操作和现象所得到的结论正确的是( )| 选项 | 实验操作 | 现象 | 结论 |
| A | 向稀HNO3中加入过量铁粉,再滴入少量KSCN溶液 | 溶液变红 | 稀HNO3将Fe氧化为Fe3+ |
| B | 向AgNO3溶液中滴加过量氨水 | 溶液澄清 | Ag+与NH3•H2O能大量共存 |
| C | 将可调高度的铜丝伸入到稀HNO3中 | 溶液变蓝 | Cu与稀HNO3发生置换反应 |
| D | 将KI和FeCl3溶液在试管中混合后,加入CCl4,振荡,静置 | 下层溶液显紫红色 | 氧化性:Fe3+>I2 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.向稀HNO3中加入过量铁粉,生成硝酸亚铁;
B.向AgNO3溶液中滴加过量氨水,生成银氨络离子;
C.稀硝酸与铜反应生成硝酸铜和NO;
D.下层溶液显紫红色,说明有碘生成.
解答 解:A.向稀HNO3中加入过量铁粉,生成硝酸亚铁,加入KSCN,溶液不变红色,故A错误;
B.向AgNO3溶液中滴加过量氨水,生成银氨络离子,则Ag+与NH3•H2O不能大量共存,故B错误;
C.稀硝酸与铜反应生成硝酸铜和NO,没有单质生成,不是置换反应,故C错误;
D.下层溶液显紫红色,说明有碘生成,可说明氧化性:Fe3+>I2,故D正确.
故选D.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、离子的检验为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 天天练口算系列答案
天天练口算系列答案
相关题目
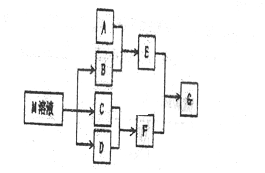
20.NiCl2是化工合成中最重要的镍源,工业上以金属镍废料(含Fe、Ca、Mg等杂质)为原料生产NiCl2,继而生产Ni2O3的工艺流程如图:

已知:1.Ksp( CaF2)=1.5×10-10Ksp(MgF2)=7.4×10-11Ksp(NiCO3)=1.42×10-7
2.流程中相关金属离子生成氢氧化物沉淀的pH如表所示:
(1)为了提高镍元素的浸出率,在“酸浸”时可采取的措施有:增大盐酸的浓度(或将镍废料研成粉末或延长浸泡时间等)(写出一种即可).
(2)加入H2O2时发生主要反应的离子方程式为2Fe2++H2O2+2H+═2Fe3++2H2O.
(3)“除铁”时,控制溶液pH的范围为3.2~7.1.
(4)滤渣B的主要成分的化学式为MgF2、CaF2.
(5)确保沉镍完全(即溶液中c(Ni2+)<1.0×10-6),保持溶液中c(CO32-)>0.142mol•L-1.
(6)“氧化”生成Ni2O3的离子方程式为2Ni2++ClO-+4OH-=Ni2O3↓+Cl-+2H2O.

已知:1.Ksp( CaF2)=1.5×10-10Ksp(MgF2)=7.4×10-11Ksp(NiCO3)=1.42×10-7
2.流程中相关金属离子生成氢氧化物沉淀的pH如表所示:
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
| 开始沉淀的pH | 1.1 | 6.5 | 7.1 |
| 沉淀完全的pH | 3.2 | 9.7 | 9.2 |
(2)加入H2O2时发生主要反应的离子方程式为2Fe2++H2O2+2H+═2Fe3++2H2O.
(3)“除铁”时,控制溶液pH的范围为3.2~7.1.
(4)滤渣B的主要成分的化学式为MgF2、CaF2.
(5)确保沉镍完全(即溶液中c(Ni2+)<1.0×10-6),保持溶液中c(CO32-)>0.142mol•L-1.
(6)“氧化”生成Ni2O3的离子方程式为2Ni2++ClO-+4OH-=Ni2O3↓+Cl-+2H2O.
18.除去酒精中混有的少量水,选用的试剂是( )
| A. | 金属钠 | B. | 浓H2SO4 | C. | 无水CaCl2 | D. | 生石灰 |
8.下列关于有机化合物的说法正确的是( )
| A. | 乙烯能够使溴水褪色,是因为乙烯和溴水反应生成了2-溴乙烷 | |
| B. | 将红热的铜丝插入到1-丙醇中,可以制得丙酮 | |
| C. | 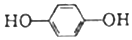 和苯酚互为同系物 和苯酚互为同系物 | |
| D. | 分子式为C10H12具有两个邻位链烃取代基的芳香烃有4种(不考虑立体异构) |
15.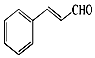 自然界中的许多植物中含有醛,其中有些具有特殊的香味,可作为植物香料使用.桂皮中含有肉桂醛,结构如图,杏仁中含有苯甲醛.以下说法错误的是( )
自然界中的许多植物中含有醛,其中有些具有特殊的香味,可作为植物香料使用.桂皮中含有肉桂醛,结构如图,杏仁中含有苯甲醛.以下说法错误的是( )
 自然界中的许多植物中含有醛,其中有些具有特殊的香味,可作为植物香料使用.桂皮中含有肉桂醛,结构如图,杏仁中含有苯甲醛.以下说法错误的是( )
自然界中的许多植物中含有醛,其中有些具有特殊的香味,可作为植物香料使用.桂皮中含有肉桂醛,结构如图,杏仁中含有苯甲醛.以下说法错误的是( )| A. | 肉桂醛分子中含有两种官能团,分子式为C9H8O | |
| B. | 肉桂醛分子中最多有18个原子共平面 | |
| C. | 1 mol肉桂醛与氢气加成时最多消耗4 mol H2 | |
| D. | 肉桂醛与苯甲醛不是同系物,但都能发生氧化反应和还原反应 |
12.下列有关实验原理或实验操作正确的是( )
| A. | 利用丁达尔效应鉴别FeCl3溶液和Fe(OH)3胶体 | |
| B. | 只能利用焰色反应可鉴别KCl溶液和Na2SO4溶液 | |
| C. | 用水润湿pH试纸测量某溶液的PH | |
| D. | 实验室用NaOH溶液除去Cl2中的少量HCl |
13.阿伏加德罗常数的值为NA.下列说法正确的是( )
| A. | 1L0.1mol•L-1NH4Cl溶液中,NH4+的数量为0.1NA | |
| B. | 2.4gMg与H2SO4完全反应,转移的电子数为0.1NA | |
| C. | 标准状况下,2.24LN2和O2的混合气体中分子数为0.2NA | |
| D. | 0.1mol H2和0.1mol I2于密闭容器中充分反应后,其分子总数为0.2NA |
 3-甲基戊烷
3-甲基戊烷 2,2-二甲基-3-乙基戊烷.
2,2-二甲基-3-乙基戊烷.