题目内容
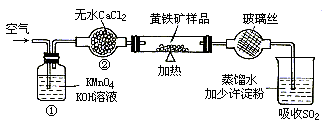
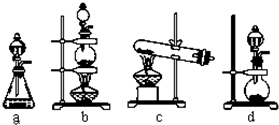
下图是一个实验室测定黄铁矿中硫的百分含量的装置.
实验时有如下操作:(A)将磁管中样品加热到800~850℃.(B)称取研细的黄铁矿样品.(C)连接全部仪器,使其成为整套实验装置,并检查气密性.(D)将样品小心放入盛器中,再将盛器小心地推入磁管中部.(E)以每分钟1 L的速度鼓入空气.(F)用标准碘液滴定含淀粉的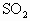 水溶液.
水溶液.
(1)正确的实验步骤,其操作编号是_________.
(2)装置①的作用是________;装置②的作用是________.
(3)应根据_________现象判断滴定已达到终点而停止鼓入空气.
(4)碘液跟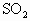 水溶液发生反应的化学方程式是_________.
水溶液发生反应的化学方程式是_________.
(5)假定矿样品的硫全部转化为二氧化硫,并全部被水吸收.著称得矿样的质量是0.12g,滴定管中碘液初读数为0.10mL,未读数为25.60mL,标准碘液的浓度为0.05mol/L,则黄铁矿样品中的含硫量是__________.
解析:
|
(1)CBDEAF (2)除去空气中的 (3)向吸收 (4) (5)34% |

 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案(1)其中“氯碱工业”就是以食盐水为原料制取Cl2等物质,有关的化学方程式为:
(2)实验室用二氧化锰制取氯气的化学方程式为:
(3)实验室中模拟Br-→Br2的转化,可以通过在KBr溶液中滴加少量新制氯水的实验进行实现.写出Br-→Br2的转化离子方程式为:
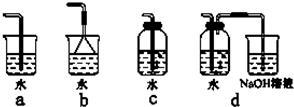
(4)实验室制备氯气的反应会因盐酸浓度下降而停止.为测定反应残余液中盐酸的浓度,探究小组同学进行了以下实验:取100mL残余液放入烧杯中,将烧杯(含玻璃棒)放在电子天平上(如下图),再把已称好50.0g CaCO3粉末慢慢加入到残余液中,边加边搅拌使其充分反应.观察读数变化如下表所示:

| CaCO3用量 | 未加CaCO3时 | 加约四分之一时 | 加一半时 | 全部加完时 |
| 读数/g | 318.3 | 325.3 | 334.5 | 359.5 |
①实验中产生的CO2气体质量为
②残余液中盐酸的物质的量浓度为(结果精确到小数点后一位)
(8分)[化学—化学与技术]
粗铜中含有少量的锌、铁、银、金等金属和少量矿物杂质(与酸不反应)。在实验室条件下以硫酸铜溶液为电解液,用电解的方法对粗铜提纯,并对阳极泥和电解液中金属进行回收和含量测定。回答以下问题;
(1)步骤一:电解精制:电解过程中,硫酸铜的浓度会 (选填:变大、不变、变小)。
步骤二:电解完成后,对电解液进行处理。
(2)阳极泥的综合利用:
稀硝酸处理阳极泥得到硝酸银稀溶液,请写出该步反应的离子方程式: 。
残渣含有极少量的黄金,如何回收金,他们查阅了有关资料,了解到了一些有关金的知识,以下是他们获取的一些信息:
| 序号 | 反应 | 平衡常数 |
| 1 | Au + 6HNO3(浓)= Au(NO3)3 + 3NO2↑+ 3H2O | << 1 |
| 2 | Au3+ + 4Cl— = AuCl4— | >>1 |
(3)电解液含量的测定:下图是该小组探究电解液的一个实验流程:
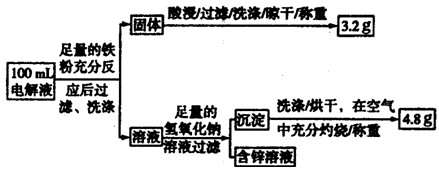
则100mL滤液中Cu2+的浓度为 mol·L—1,Fe2+的浓度为 mol·L—1
(8分)[化学—化学与技术]
粗铜中含有少量的锌、铁、银、金等金属和少量矿物杂质(与酸不反应)。在实验室条件下以硫酸铜溶液为电解液,用电解的方法对粗铜提纯,并对阳极泥和电解液中金属进行回收和含量测定。回答以下问题;
(1)步骤一:电解精制:电解过程中,硫酸铜的浓度会 (选填:变大、不变、变小)。
步骤二:电解完成后,对电解液进行处理。
(2)阳极泥的综合利用:
稀硝酸处理阳极泥得到硝酸银稀溶液,请写出该步反应的离子方程式: 。
残渣含有极少量的黄金,如何回收金,他们查阅了有关资料,了解到了一些有关金的知识,以下是他们获取的一些信息:
|
序号 |
反应 |
平衡常数 |
|
1 |
Au + 6HNO3(浓)= Au(NO3)3 + 3NO2↑+ 3H2O |
<< 1 |
|
2 |
Au3+ + 4Cl— = AuCl4— |
>>1 |
从中可知,金很难与硝酸反应,但却可溶于王水(浓硝酸与盐酸按体积比l:3的混合物).请你简要解释金能够溶于王水的原因 。
(3)电解液含量的测定:下图是该小组探究电解液的一个实验流程:

则100mL滤液中Cu2+ 的浓度为 mol·L—1 ,Fe2+的浓度为 mol·L—1
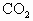 和还原性气体;净化空气;吸收水蒸气,干燥空气.
和还原性气体;净化空气;吸收水蒸气,干燥空气.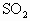 的液体中滴加碘液后溶液变蓝,至不褪色.
的液体中滴加碘液后溶液变蓝,至不褪色.