题目内容
(15分)
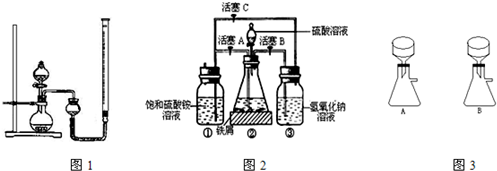
请设计实验:用MnO2与浓盐酸制备纯净、干燥的Cl2,其他药品与试剂任选。
(1)写出该反应的化学方程式 。 (2)在下面方框中,A表示有分液漏斗和圆底烧瓶组成的气体发生器,请在虚线框内的A后完成该反应的实验装置示意图(夹持装置、连接胶管不必
(2)在下面方框中,A表示有分液漏斗和圆底烧瓶组成的气体发生器,请在虚线框内的A后完成该反应的实验装置示意图(夹持装置、连接胶管不必 画出,需要加热的仪器下方用△标出),按气流方向在每件仪器下方标出字母B、C……;其他可选用的仪器(数量不限)简易表示如
画出,需要加热的仪器下方用△标出),按气流方向在每件仪器下方标出字母B、C……;其他可选用的仪器(数量不限)简易表示如 下:
下:
(3)根据方框中的装置图,完成下表(若无需填写,则在表格中写“无”)
| 仪器符号 | 仪器中所加物质 | 作用 |
| A | MnO2、浓盐酸 | MnO2与浓盐酸生成Cl2 |
| | | |
| | | |
| | | |
| | | |
(5)请写出Cl2在工业、农业、医疗、卫生等方面的用途 。(写出两种即可)
(6)将Cl2与SO4分别通人品红溶液,都能使品红褪色。简述用褪色的溶液区别二者的实验方法。
(1)MnO2+4HCl(浓)
(2)(3分)
(3)(4分)
(4)2MnO4+16H++10Cl-仪器符号 仪器中所加物质 作用 B 饱和食盐水 除去Cl2中的HCl C 浓硫酸 除去Cl2中的H2O D 无 收集氯气 E NaOH溶液 尾气处理,防止环境污染 
(5)自来水消毒、制农药、塑料等(2分)
(6)取适量的已褪色的品红溶液于试管中,用酒精灯加热。若品红溶液颜色复原为红色,则为SO2使其褪色;若品红溶液颜色仍为无色,则为C12使其褪色。(2分)
解析

练习册系列答案
相关题目