��Ŀ����
���������������( )
A��10mL��������Ϊ98%��H2SO4����10mLˮϡ�ͺ�H2SO4��������������49%
B������0.1mol/L��Na2CO3��Һ480ml������500ml����ƿ
C���ڱ���£���22.4L��������1Lˮ�У��õ�1mol/L�İ�ˮ
D�������ȷݲ����͵��ռ���Һ�зֱ����һ������Na2O2��Na2O��ʹ��Һ��ǡ�ñ��ͣ�������Na2O2��Na2O�����ʵ���֮�ȵ���1��1(�����¶Ȳ���)
��ϰ��ϵ�д�
�����Ŀ
20�� ����������һ�ָ�Ч��ɫ�������������ڷ�ˮ��������ˮ�Ĵ������ӻ��������ĽǶȿ����Ʊ��������νϺõķ���Ϊ��ⷨ��Fe+2H2O+2OH$\frac{\underline{\;ͨ��\;}}{\;}$FeO42-+3H2��������ԭ����ͼ��ʾ����֪��Na2FeO4ֻ��ǿ�����������ȶ����ױ�H2��ԭ������˵����ȷ���ǣ�������
����������һ�ָ�Ч��ɫ�������������ڷ�ˮ��������ˮ�Ĵ������ӻ��������ĽǶȿ����Ʊ��������νϺõķ���Ϊ��ⷨ��Fe+2H2O+2OH$\frac{\underline{\;ͨ��\;}}{\;}$FeO42-+3H2��������ԭ����ͼ��ʾ����֪��Na2FeO4ֻ��ǿ�����������ȶ����ױ�H2��ԭ������˵����ȷ���ǣ�������
 ����������һ�ָ�Ч��ɫ�������������ڷ�ˮ��������ˮ�Ĵ������ӻ��������ĽǶȿ����Ʊ��������νϺõķ���Ϊ��ⷨ��Fe+2H2O+2OH$\frac{\underline{\;ͨ��\;}}{\;}$FeO42-+3H2��������ԭ����ͼ��ʾ����֪��Na2FeO4ֻ��ǿ�����������ȶ����ױ�H2��ԭ������˵����ȷ���ǣ�������
����������һ�ָ�Ч��ɫ�������������ڷ�ˮ��������ˮ�Ĵ������ӻ��������ĽǶȿ����Ʊ��������νϺõķ���Ϊ��ⷨ��Fe+2H2O+2OH$\frac{\underline{\;ͨ��\;}}{\;}$FeO42-+3H2��������ԭ����ͼ��ʾ����֪��Na2FeO4ֻ��ǿ�����������ȶ����ױ�H2��ԭ������˵����ȷ���ǣ�������| A�� | b�ǵ�Դ������ | |
| B�� | �����缫��ӦΪFe-6e-+4H2O�TFeO42-+8H+ | |
| C�� | �������У���Ҫ���������������弰ʱ�ų� | |
| D�� | ����·��ͨ��1mol���ӵĵ���ʱ������11.2L��H2���� |
2�� ��һ��þ���Ͻ�Ͷ�뵽1mol/L ��������Ͻ���ȫ�ܽ������Һ�����1mol/L NaOH��Һ�����ɳ��������ʵ��������NaOH��Һ����仯�Ĺ�ϵ����ͼ��ʾ������˵���в���ȷ���ǣ�������
��һ��þ���Ͻ�Ͷ�뵽1mol/L ��������Ͻ���ȫ�ܽ������Һ�����1mol/L NaOH��Һ�����ɳ��������ʵ��������NaOH��Һ����仯�Ĺ�ϵ����ͼ��ʾ������˵���в���ȷ���ǣ�������
 ��һ��þ���Ͻ�Ͷ�뵽1mol/L ��������Ͻ���ȫ�ܽ������Һ�����1mol/L NaOH��Һ�����ɳ��������ʵ��������NaOH��Һ����仯�Ĺ�ϵ����ͼ��ʾ������˵���в���ȷ���ǣ�������
��һ��þ���Ͻ�Ͷ�뵽1mol/L ��������Ͻ���ȫ�ܽ������Һ�����1mol/L NaOH��Һ�����ɳ��������ʵ��������NaOH��Һ����仯�Ĺ�ϵ����ͼ��ʾ������˵���в���ȷ���ǣ�������| A�� | ����Al��OH��3�������������Ϊ0.78g | B�� | ����70ml NaOH ʱ��Һ�ʼ��� | ||
| C�� | $\frac{n��Mg��}{n��Al��}$�����ֵΪ1.5 | D�� | a��ȡֵ��ΧΪ0��a��45mL |
19������ʵ�鷽������������ۺ������ǣ�������
| A�� | B�� | C�� | D�� |
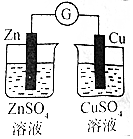 |  |  |  |
| ��֤��ѧ��ת��Ϊ���� | ��֤�����ԣ�Cl2��Br2��I2 | ��֤�¶ȶ�ƽ���ƶ���Ӱ�� | ��ȡMgCl2���� |
| A�� | A | B�� | B | C�� | C | D�� | D |




 ��SO42-
��SO42-

 ������ͼ��ʾ��A��B��C��D��E�������ʵ��ת����ϵ��������Ҫ����д��Ӧ�����ʺ��йط�Ӧ�Ļ�ѧ����ʽ��
������ͼ��ʾ��A��B��C��D��E�������ʵ��ת����ϵ��������Ҫ����д��Ӧ�����ʺ��йط�Ӧ�Ļ�ѧ����ʽ��