题目内容
【题目】(1)有①168 O 、 17 8O 、 188O ;②H2、D2、T2;③石墨、金刚石;④11H 、21H、 31H;四组微粒或物质。互为同位素的是_____(填编号)。
(2)下列物质中:①N2;②MgCl2;③NH4Cl;④CH4;⑤CO2;⑥Ne;⑦H2S;⑧KOH;⑨Na2O2; ⑩K2O;只存在共价键的是_____;属于离子化合物,但含有共价键的 是_____。
(3) 用电子式表示下列物质:
MgCl2 _____; N2 _____;
NH4+_____; Na2O2 _____。
【答案】①、④ ①、④、⑤、⑦ ③、⑧、⑨ ![]()
![]()
![]()
【解析】
(1)质子数相同,中子数不同的原子互为同位素;
(2)像氯化氢那样,以共用电子对(或共价键)结合在一起的化合物,叫做共价化合物;离子化合物 由阳离子和阴离子构成的化合物;
(3)根据构成物质的化学键进行判断并书写电子式。
(1)①168 O 、 17 8O 、 188O质子数相同,中子数不同,故互为同位素;
②H2、D2、T2是由氢的同位素原子构成的氢分子,既不是同位素,也不是同素异形体;
③石墨、金刚石都是由碳元素形成的不同单质,互为同素异形体;
④11H 、21H、 31H质子数相同,中子数不同,故互为同位素;
互为同位素的是:①④;
(2)①CO2中只含共价键,为共价化合物;
②MgCl2中只含离子键,为离子化合物;
③NH4Cl中含离子键和N-H极性共价键,为离子化合物;
④CH4中只含共价键,为共价化合物;
⑤CO2中只含共价键,为共价化合物;
⑥Ne中不含化学键,为单质;
⑦H2S中只含极性共价键,为共价化合物;
⑧KOH中含离子键和极性共价键,为离子化合物;
⑨Na2O2中含离子键和O-O非极性共价键,为离子化合物;
⑩K2O中只含离子键;
只存在共价键的是①④⑤⑦;
属于离子化合物的是②③⑧⑨⑩,且含有共价键为:③⑧⑨;
(3)MgCl2是镁离子与2个氯离子通过离子键结合,电子式为:![]() ;
;
氮气中两个氮原子通过三对共用电子对结合,电子式为:![]() ;
;
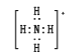
氨根离子为阳离子,氮原子与氢原子间通过共价键,电子式为: ;
;
过氧化钠为离子化合物,2个钠离子与过氧根离子通过离子键结合,两个氧原子通过共用电子对结合,电子式为:![]() 。
。