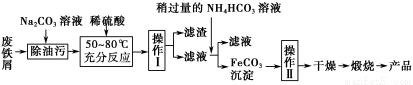
题目内容
下列各图示中能较长时间看到Fe(OH)2白色沉淀的是 ( )。
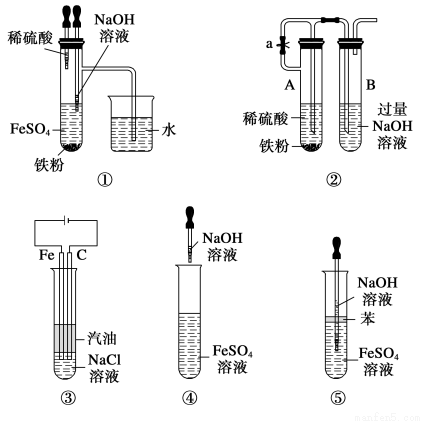
A.①②③④⑤ B.①②③⑤
C.①②③④ D.②③④⑤
B
【解析】因为Fe(OH)2在空气中很容易被氧化为红褐色的Fe(OH)3,即发生4Fe(OH)2+O2+2H2O=4Fe(OH)3。因此要较长时间看到Fe(OH)2白色沉淀,就要排除装置中的氧气或空气。①、②原理一样,都是先用氢气将装置中的空气排尽,并使生成的Fe(OH)2处在氢气的保护中;③的原理为铁作阳极产生Fe2+,与电解水产生的OH-结合生成Fe(OH)2,且液面用汽油保护,能防止空气进入;⑤中液面加苯阻止了空气进入;④由于空气中的氧气,能迅速将Fe(OH)2氧化,因而不能较长时间看到白色沉淀。

练习册系列答案
相关题目