题目内容
(5分)氰[(CN)2]为无色可燃气体、剧毒、有苦杏仁味,是拟卤素的一种。拟卤素的性质与卤素相似。
(1)写出氰与苛性钠溶液反应的化学方程式: 。
(2)已知氰分子中键角为180°,分子具有对称性,(CN)2的结构式为 ,(CN)2的分子为(填“极性”或“非极性”) 分子。
(3)CN-中电子数为 。
(1)(CN)2 + 2NaOH = NaCN + NaCNO + H2O(2分)
(2)N≡C—C≡N (1分);非极性 (1分);
(3)14(1分);
解析:略

练习册系列答案
 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案
相关题目
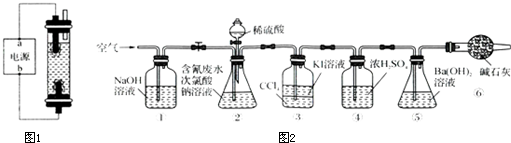

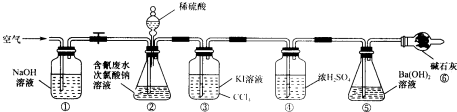
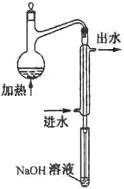 Ag++2CN - == [Ag(CN)2] -
Ag++2CN - == [Ag(CN)2] -