题目内容
某校化学研究学习小组设计如下实验方案,测定小苏打样品中纯碱的质量分数.
(1)方案一:称取一定质量的样品,置于坩埚中加热至恒重后,冷却,称量剩余固体质量,计算.实验中反应化学方程式为________.
(2)方案二:按下图装置进行实验,已知B中盛放的是浓H2SO4.回答以下问题:
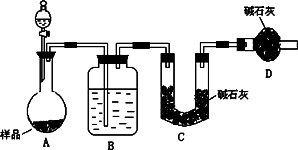
①实验加入药品前应先________________.分液漏斗中应该装________(填“盐酸”或“稀硫酸”).D装置的作用是________________.
②实验中除称量样品质量外,还需称________装置(用字母表示)前后质量的变化.
③根据此实验得到的数据,测定结果有较大误差.因为实验装置还存在一个明显缺陷,该缺陷是________________.
(3)方案三:称取一定量样品,置于小烧杯中,加适量水溶解,向小烧杯中加入足量氯化钡溶液,过滤、洗涤、干燥沉淀,称量固体质量,计算.
①过滤操作中,除了烧杯、漏斗外还用到的玻璃仪器是________.
②若加入试剂改为氢氧化钡,已知称得样品9.5 g,干燥的沉淀质量为19.7 g,则样品中碳酸钠的质量分数为________(保留一位小数).
答案:

练习册系列答案
相关题目
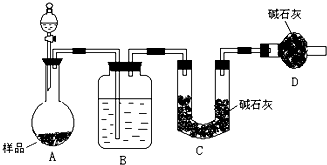 某校化学研究学习小组设计如下实验方案,测定小苏打样品中纯碱的质量分数.
某校化学研究学习小组设计如下实验方案,测定小苏打样品中纯碱的质量分数.


