题目内容
|
如图装置中,甲、乙两烧杯中都盛有同体积的0.1 mol/L的硫酸溶液.下列有关实验的叙述中,错误的是
| |
A. |
电流计G的指针不动 |
B. |
通过电流计G的电子流动方向是由上向下 |
C. |
甲、乙两装置都不是电解槽 |
D. |
甲装置中铜极上有气泡产生 |
E. |
乙装置中,c(H+)会减小 |
答案:DE
解析:
解析:
|
甲乙两池均是原电池装置,电流计是外电路,Cu是电源的正极,Zn是电源的负极,所以通过电流计G的电子流动方向是从下到上,Cu片上有气泡冒出,H+浓度均会减小. |

练习册系列答案
相关题目
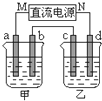 如图所示的装置中,甲、乙两烧杯中分别盛放有足量的CuSO4溶液和100g 10.00%的K2SO4溶液,a、b、c、d均为石墨电极.接通电源一段时间后,测得乙中K2SO4溶液浓度为10.47%,甲中a电极的质量增加.下列说法正确的是( )
如图所示的装置中,甲、乙两烧杯中分别盛放有足量的CuSO4溶液和100g 10.00%的K2SO4溶液,a、b、c、d均为石墨电极.接通电源一段时间后,测得乙中K2SO4溶液浓度为10.47%,甲中a电极的质量增加.下列说法正确的是( )| A、甲、乙溶液的pH均减小 | B、电极b上生成气体的体积约为2.8L(标准状况下) | C、电极d上发生的反应为:2H2O+2e-?H2↑+2OH- | D、欲使甲中的溶液恢复至原来的浓度,可加入24.5g的Cu(OH)2 |
 如图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都有明显的胀大(忽略液体体积对气球的影响).则所用试剂可能分别依次是( )
如图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都有明显的胀大(忽略液体体积对气球的影响).则所用试剂可能分别依次是( )| A、甲:浓硫酸和木炭 乙:浓氨水和HBr | B、甲:双氧水和MnO2 乙:NaOH溶液和NO2 | C、甲:苯酚和Na2CO3溶液 乙:NaOH溶液和Cl2 | D、甲:浓硫酸和蔗糖(滴有几滴水) 乙:水和氨气 |

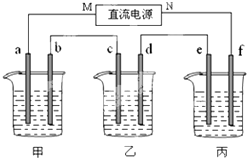 如图所示装置中,甲、乙两个烧杯分别依次盛放200mL饱和食盐水、足量的AgNO3溶液,a、b、c、d四个电极均为石墨电极.接通电源,经过一段时间后,测得乙中d电极质量增加了2.16g.据此回答问题:
如图所示装置中,甲、乙两个烧杯分别依次盛放200mL饱和食盐水、足量的AgNO3溶液,a、b、c、d四个电极均为石墨电极.接通电源,经过一段时间后,测得乙中d电极质量增加了2.16g.据此回答问题: 如图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都明显胀大(忽略液体体积对气球体积的影响).则滴管和烧瓶中所用试剂可能是( )
如图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都明显胀大(忽略液体体积对气球体积的影响).则滴管和烧瓶中所用试剂可能是( )