题目内容
下列表述中正确的是( )
| A.任何能使熵值减小的过程都能自发进行 |
| B.1mol NaOH分别和1mol CH3COOH、1molHNO3反应,后者比前者△H小 |
C.已知热化学方程式2SO2(g)+O2(g) 2SO3(g);△H=-Q kJ·mol-1(Q>0),则将2mol SO2(g)和1 mol O2(g)置于一密闭容器中充分反应后放出Q kJ的热量 2SO3(g);△H=-Q kJ·mol-1(Q>0),则将2mol SO2(g)和1 mol O2(g)置于一密闭容器中充分反应后放出Q kJ的热量 |
| D.在Na2SO4溶液中加入过量的BaCl2后,溶液中不存在SO42- |
B
解析试题分析:A项: 事实上熵变和焓变都不能完全解释自发反应,一般会用吉布斯自由能来判别反应是否可以自发进行,△G=△H-T△S,当△G>0时,反应可逆向进行,△G=0时,反应平衡,当△G<0时反应可正向进行,故A错;
C项:反应为可逆反应,不能进行到底,放出的热量要小于Q kJ,故错;
D项:BaSO4虽是难容物,但也存在溶解平衡,溶液肯定存在较少的SO42-,故错。
故选B。
考点:熵的 热化学方程式的书写 △H的计算 离子反应
点评:本题比较典型,全面考查了熵的知识、热化学方程式的书写、△H的计算、离子反应等,仔细研究,定会有所提高。

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案
相关题目
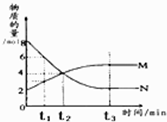 在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )| A、反应的化学方程式为:N?2M | B、t2时,反应不再发生 | C、t2时,正反应速率等于逆反应速率 | D、t3后,反应到达最大限度 |
 在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )